نيم رساناها
معمولاُ اجسام از لحاظ عبور يا عدم عبور الکتريسيته به دو دسته رسانا و عايق تقسيم ميشود. اما گروه ديگري از اجسام نيز وجود دارد که به طور کامل رسانا و نه به طور کامل نارسانا ست. اين گروه خاص از اجسام را نيم رسانا ميگويند.
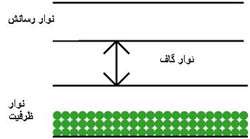
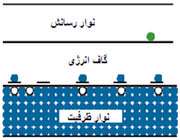
ترازهاي انرژي الکترون در جسم جامد تشکيل نوارهايي مي دهند هر نوار شامل تعداد بسيار زيادي ترازهاي گسسته است که بسيار نزديک به هم مي باشند. در مبحث نيم رساناها بالاترين نوار پر را نوار ظرفيت و پايين ترين نوارخالي را نوار رسانش مي نامند و به فاصله بين اين دو نوار ناحيه ممنوع يا گاف انرژي مي گويند و در اين ناحيه هيچ تراز انرژي وجود ندارد.
مقدار گاف انرژي نقش تعيين کننده اي در خواص نيم رساناها دارد.
انواع نيم رساناها
نيم رسانا ذاتي
در برخي از نيم رساناها گاف انرژي بين نوار رسانش و نوار ظرفيت به قدر کافي کوچک است که تعدادي از الکترون هاي نوار ظرفيت در دماي اتاق نيز، با برانگيختگي گرمايي، انرژي لازم براي گذر از نوار ظرفيت به نوار رسانش را به دست مي آورند به اين گونه نيم رساناها، نيم رساناي ذاتي مي گويند.
نيم رساناي غير ذاتي
در بيشتر نيم رساناها که غير ذاتي ناميده ميشوند، اندازه گاف نواري، با افزودن دقيق ناخالصي هايي کنترل ميشود، که اين فرآيند تقويت ناميده ميشود. سيستم عمل تقويت روي سيليکون يکي از متداولترين نيم رساناهاست.
براي مثال سيلسيوم و ژرمانيوم دو ماده نيم رسانا هستند اتم هاي هر دوي اين عنصرها، چهار الکترون ظرفيت دارند. در هر يک از اين نيم رساناها اگر به جاي يکي از اين اتم ها يک اتم ناخالص يا سه ظرفيتي وارد کنيم، نيم رسانا را آلاييده ايم و به ترتيب نيم رساناي غير ذاتي نوع N و نوع P به دست آورده ايم.
نيم رساناي نوع n
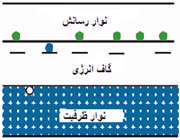
وقتي به سيليکون، ناخالصي فسفر افزوده شود، تراز انرژي اتمي فسفر، دقيقا در زير نوار رسانش سيليکون قرار ميگيرد.
هر اتم فسفر، 4 الکترون از 5 الکترون ظرفيتش را تشکيل نمونه با 4 اتم si مجاور به کار ميبرد و انرژي گرمايي به تنهايي کافي است تا باعث شود، الکترون اضافي ظرفيت به نوار رسانش بر انگيخته شده به يک يون p غير متحرک را بر جاي گذارد. اتم هاي فسفر ، دهنده ناميده ميشود.
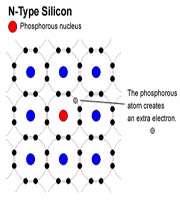
رسانش الکتريکي در اين نوع نيم رسانا عمدتاً در اثر حرکت الکترون هاي حاصل از اتم هاي دهنده در نوار رسانش، به وجود ميآيد. اين نوع نيم رسانا نوع n ناميده مي شود که در آن n به معني منفي است، اين نوعي بار الکتريکي که توسط الکترون ها حمل ميشود.
نيم رساناي نوع p
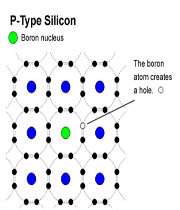
وقتي به سيليکون ناخالص آلومينيم افزوده ميشود. تراز انرژي اتم هاي AL که اتم هاي پذيرنده ناميده ميشوند، درست بالاي نوار ظرفيت سيليکون قرار ميگيرد. با سه اتم Si مجاور پيوند جفت الکتروني منظمي تشکيل ميدهد. اما با چهارمين اتم Si فقط يک پيوند تک الکتروني تشکيل ميدهد.

يک الکترون به راحتي از نوار ظرفيت يک اتم آلومينيوم در تراز پذيرنده بر انگيخته ميشود. در نهايت، يک يون منفي تا A غير متحرک به وجود ميآمد و در نتيجه اين فرآيند يک حفره مثبت در نوار ظرفيت پديدار ميشود. از آن جا که رسانش الکتريکي در اين نوع نيم رسانا عمدتاً شامل حرکت حفره هاي مثبت است اين نوع نيم رسانا، نوع P ناميده ميشود.
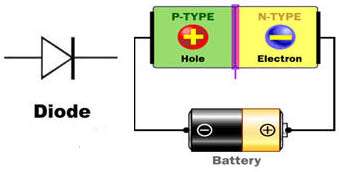
ديود
ديود از اتصال يك نيمه هادي نوع N و يك نيمه هادي نوع P به وجود مي آيد و با حرف D نشان داده مي شود . ديودها جريان الکتريکي را در يک جهت از خود عبور ميدهند و در جهت ديگر در مقابل عبور جريان از خود مقاومت بالايي نشان ميدهند.
اين خاصيت آن ها باعث شده بود تا در سال هاي اوليه ساخت اين وسيله الکترونيکي، به آن دريچه يا Valve هم اطلاق شود. از لحاظ الکتريکي يک ديود هنگامي عبور جريان را از خود ممکن ميسازد که شما با برقرار کردن ولتاژ در جهت درست (قطب مثبت پيل به آند و قطب منفي به کاتد) آن را آماده کار کنيد. مقدار ولتاژي که باعث ميشود تا ديود شروع به هدايت جريان الکتريکي نمايد ولتاژ آستانه يا (forward voltage drop) ناميده ميشود که چيزي حدود 0.6 تا 0.7 ولت ميباشد.
برچسبها:
هواي مرطوب
باور غلط : هواي مرطوب، رساناي جريان الکتريکي است.

شايد شما هم ديده باشيد که برخي از آزمايش هاي الکتروستاتيک در هواي مرطوب به خوبي کار نمي کنند و شايد در برخي کتاب ها ديده ايد که گفته شده آب موجود در هواي مرطوب باعث رسانايي هوا مي شود. در واقع اين اشتباه از آنجا رخ مي دهد که برخي فکر مي کنند که به دليل اينکه آب ناخالص رسانا است و اين رسانا در هواي مرطوب وجود دارد، باعث مي شد که هوا نيز رسانا شود.
ولي اگر مقداري با مفاهيم الکتريسته آشنايي داشته باشيد، مي دانيد که اگر بخواهيم هوا را رسانا کنيم، بايد آن را پر از ذرات باردار متحرک کنيم. در حالي که بخار آب (که در هواي مرطوب وجود دارد) از ذرات باردار (يون ها) ساخته نشده و بخار آب، از لحاظ بار الکتريکي خنثي است، پس وجود بخار آب زياد در محيط باعث زياد شدن هدايت الکتريکي آن نمي شود. حتي قطرات معلق آب مايع که در مِه وجود دارد نيز خنثي است و تاثيري در کم يا زياد شدن خاصيت رسانايي هوا ندارد.
براي اينکه مِه باعث رسانا شدن محيط شود بايد قطرات آب هر کدام داراي بار الکتريکي باشند. که در واقع اين طور نيست.
شايد گاهي اوقات شما هم نگران اين موضوع بوديد که وجود غبار در حمام باعث برق گرفتگي شما شود، پس با اين توضيحات متوجه شديد که نبايد نگراني در اين زمينه براي شما وجود داشته باشد.
رسانا، نارسانا
در برخي مواد، مانند فلزات، شير آب و بدن انسان، مقداري الکترون مي توانند تقريباً آزادانه حرکت کند. چنين موادي را رسانا مي ناميم. در مواد ديگري مانند شيشه، آب خالص از نظر شيميايي و پلاستيک، هيچ کدام از بارها نمي توانند آزادانه حرکت کنند. چنين مادي را نارسانا و يا عايق مي ناميم.
اگر در حالي که يک ميله مسي را در دست داريد آن را با پشم مالش دهيد، نمي توانيد ميله را باردار کنيد، چون شما و ميله هر دو رسانا هستيد. اين مالش موجب عدم توازن بار در ميله مي شود، ولي بار اضافي بي درنگ از طريف بدن شما به کف (که به سطح زمين متصل است) منتقل شده و ميله به سرعت خنثي مي شود.

با برقراري مسيري از رساناها بين يک جسم و سطح زمين، مي گوييم جسم به زمين متصل شده است. در خنثي سازي جسم، مي گوييم جسم بي بار شده است. اگر به جاي اين که ميله را در دست خود بگيريد، آن را از طريق يک عايق در دست داشته باشيد، مسير رسانا با زمين از بين مي رود و تا زماني که آن را به طور مستقيم با دست خود نگرفته ايد، ميله با مالش مي تواند باردار شود.
خواص رساناها و عايق ها ناشي از ساختار اتمي و سرشت الکتريکي آن هاست.
اتم ها داراي پروتون هايي با بار مثبت، الکترون هايي با بار منفي و نوترون هايي با بار خنثي هستند. پروتون ها و نوترون ها در هسته مرکزي، کنار هم قرار دارند، در مدل ساده اتم، الکترون ها گرد هسته مي چرخند.
بار الکترون تنها و همچنين پروتون تنها از نظر اندازه يکسان ولي علامت آن ها مخالف يکديگر است. از اين رو اتمي که از نظر الکتريکي خنثي است، تعداد الکترون ها و پروتون هاي برابري دارد. الکترون ها در نزديکي هسته ها قرار دارند. چون علامت الکتريکي آن ها مخالف با علامت پروتون هاي هسته است در نتيجه به سوي هسته جذب مي شوند.
وقتي اتم هاي يک رسانا مانند مس جسم جامدي را تشکيل دهند، برخي از الکترون هاي لايه بيروني (که خيلي ضعيف به آن پيوسته اند) وابسته به اتم هاي منفرد باقي نمي مانند و بنابراين درون جامد سرگردان مي شوند و اتم هاي باردار مثبت ( يون هاي مثبت) به جا مي گذارند. الکترون هاي در حال حرکت را الکترون هاي رسانش مي ناميم. (در صورت وجود) تعداد الکترون هاي آزاد کمي در يک نارسانا وجود دارد.

نيم رساناها
نيم رساناها، مانند سيلسيم و ژرمانيم، موادي هستند که حالت ميانه رساناها و عايق ها را دارند. تحول ميکروالکترونيکي که زندگي ما را تغيير داده است به واسطه دستگاه هايي است که از مواد نيم رسانا ساخته شده است.
ابررساناها
بالاخره ابررساناهايي وجود دارند که در مقابل حرکت بار الکتريکي در آن ها هيچ مقاومتي از خود نشان نمي دهند. هنگامي که بار در يک ماده حرکت مي کند، مي گوييم جريان الکتريکي در آن ماده وجود دارد. مواد معمولي، حتي رساناهاي خوب در برابر عبور بار از خود مقاومت نشان مي دهند. ولي در يک ابر رسانا، مقاومت خيلي کم نيست، بلکه دقيقاً صفر است. اگر جرياني را در يک حلقه ابر رسانا برقرار کنيم، بدون اينکه باتري يا منبع ديگري از انرژي براي نگهداري اين جريان لازم باشد جريان الکترون ها بدون تغيير ادامه مي يابد.

آزمايشي براي تشخيص رسانايي مواد
شما مي توانيد با ساخت يک مدار ساده الکتريکي به بررسي خاصيت رسانايي الکتريکي مواد اطراف خود بپردازيد. براي اين کار نياز به سيم، باتري و يک سرپيچ و لامپ داريد، کافي است که يک سر باتري را به وسيله سيم به يک پايه سرپيچ لامپ ببنديد و به سر ديگر باتري سيمي را وصل نمائيد، به سر ديگر سرپيچ لامپ نيز سيم ديگر وصل کنيد، براي آزمايش مدار خود دو سر اين سيم را به يکديگر وصل کنيد، مشاهده مي کنيد که لامپ روشن خواهد شد.
که اين نشان دهنده اين موضوع است که سيم مسي رساناي جريان الکتريکي است، حال اين دو سيم را از هم جدا کرده و در بين آن ها اجسام مورد نظر خود را قرار دهيد، مثلاً مي توانيد دو سر اين سيم را به يک قطعه چوب، آب، يک قطعه فلز و ديگر اجسام مورد نظر خود وصل کنيد و مشاهده کنيد که در کدام حالت لامپ روشن خواهد شد.
اين آزمايش را در هواي مرطوب نيز انجام دهيد، مثلاً مدار الکتريکي خود را به داخل يک حمام آب گرم ببريد، ببينيد که وقتي مدار در اين فضا قرار مي گيرد آيا لامپ روشن خواهد شد يا خير. اين هم روشي ديگري است که ببنيد که هواي مرطوب رساناي جريان الکتريکي نمي باشد.
برچسبها:
ایزوبارها
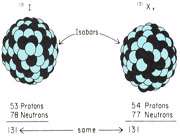
نوکلئیدهایی که عدد جرمی (تعداد کل نوترون و پروتون) یکسانی دارند، اما اعداد اتمی آن ها متفاوت است، ایزوبار نامیده می شوند. همان گونه که در شکل زیر نشان داده شده است، I-131 و Xe-131 ایزوبار های یکدیگرند. یک جفت ایزوبار نمی تواند به عنصر شیمیایی یکسانی تعلق داشته باشد. رابطه ی بین چند ایزوبار در نمودار نوکلئیدی زیر نشان دهنده ی آلومینیوم- 29 ، سیلیکون- 29، فسفر- 29 و گوگرد- 29 است.
رابطه ی بین چند ایزوبار در نمودار نوکلئیدی
توجه عمده ی ما به ایزوبارها آن است که در بیش تر تبدیلات رادیواکتیوی، یک نوکلئید به ایزوبار خودش تغییر خواهد یافت؛ به عنوان مثال I-131 نشان داده شده در شکل زیر، رادیواکتیو است و هنگامی که متحمل تغییرات عادی رادیواکتیوی خود می شود، به Xe-131 تبدیل می شود.
ایزومرها
هسته ها می توانند ترکیب پروتون - نوترون مشابهی داشته باشند اما کاملاً یکسان نباشند؛ به عنوان مثال، یک هسته می تواند انرژی بیش تری نسبت به هسته ی دیگر داشته باشد.
دو هسته ای که می توانند ترکیب یکسانی داشته باشند اما انرژی آن ها در حال تغییر است، ایزومر هم نامیده می شوند. یک مثال برای جفت ایزومری در شکل 6 نشان داده شده است؛ تکنسیم- 99 می تواند در دو حالت انرژی وجود داشته باشد: انرژی بالاتر برای این عنصر، یک حالت موقتی است و به حالت نیمه پایدار اشاره دارد .
نشانه ی یک نوکلئید در حالت نیمه پایدار، اضافه کردن حرف m به عدد جرمی است (Tc-99m) . هسته ها در حالت نیمه پایدار، انرژی و بار اضافی خود را در نهایت به دیگر ایزومرهای خود می دهند. چنین تبدیلات ایزومری در پزشکی هسته ای نقش مهمی دارند و در ادامه ی بحث با جزئیات بیش تری مورد بحث قرار خواهند گرفت.
ایزوتون ها
نوکلئیدهایی که تعداد نوترون مشابهی دارند، ایزوتون نامیده می شوند. به دلیل این که با این مطلب معمولاً در پزشکی هسته ای مواجه نمی شویم، این بحث را به اتمام می رسانیم.
برچسبها:
انرژي هاي يونش بالاتر
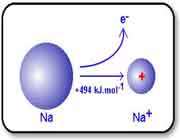
با اندکي مطالعه راجع به انرژي يونش و تشکيل يون هاي مختلف عناصر، متوجه مي شويد که سديم، منيزيم و آلومينيوم يون هاي Na+ و Mg2+ و Al3+ تشکيل مي دهند. اما آيا تا کنون از خود پرسيده ايد که چرا سديم، يون هاي Na2+ يا حتي Na3+ تشکيل نمي دهد؟
جواب اين سؤال مي تواند از انرژي دومين، سومين و ... يونش عناصر به دست آيد. به عنوان مثال، انرژي اولين يونش سديم، انرژي لازم براي برداشتن يک الکترون از يک اتم سديم خنثي است:
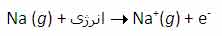
انرژي دومين يونش سديم، انرژي لازم براي برداشتن يک الکترون ديگر از يون Na+ در حالت گازي است که يک يونNa2+تشکيل مي دهد:
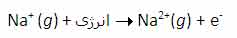
سومين انرژي يونش سديم نيز به همين ترتيب است:
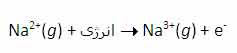
بنابراين انرژي لازم براي تشکيل يون Na3+ در فاز گازي، جمع انرژي هاي يونش اول، دوم و سوم اين عنصر است.
براي کندن يک الکترون از اتم سديم و تشکيل يون Na+ با آرايش الکتروني لايه پر، انرژي چندان زيادي لازم نيست اما وقتي يک بار اين اتفاق افتاد، براي برداشتن دومين الکترون از سديم تقريباً بايد 10 برابر انرژي يونش اوليه، انرژي صرف شود تا آرايش لايه پر Na+ شکسته شود و Na2+ تشکيل شود. به دليل اين که انرژي زيادي براي برداشتن دومين الکترون سديم در هر واکنش شيميايي لازم است، سديم مي تواند با عناصر ديگر طوري واکنش دهد که ترکيباتي شامل يون هاي Na+ تشکيل دهد نه يون هاي Na2+ يا Na3+.
اولين، دومين، سومين و چهارمين انرژي يونش سديم، منيزيوم و آلومينيوم (KJ/mol)
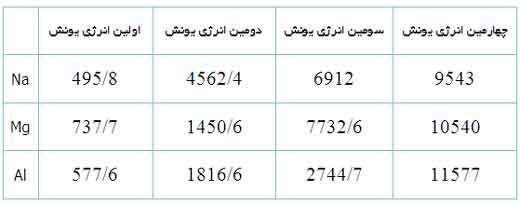
به دليل اين منيزيوم، يک پروتون بيش تر از سديم دارد، اولين انرژي يونش آن بيش تر است تا الکترون ها در اوربيتال 3s نگه دارد:
دومين انرژي يونش منيزيوم بزرگ تر از انرژي اولين يونش آن است زيرا هميشه برداشتن يک الکترون از يوني با بار مثبت، انرژي بيش تري مي گيرد تا بخواهيم همين اکترون را از يک اتم خنثي برداريم. سومين انرژي يونش منيزيوم خيلي زياد است زيرا Mg2+ آرايش پايدار و لايه پر دارد.
همين وضعيت راجع به آلومينيوم وجود دارد که اولين انرژي يونش آن از منيزيوم کم تر است. انرژي دومين و سومين يونش آلومينيوم از انرژي اولين يونش آن بزرگ تر است. اگرچه برداشتن سه الکترون از اتم آلومينيوم براي تشکيل يون Al3+مقدار انرژي زيادي لازم دارد اما انرژي لازم براي شکستن آرايش الکتروني پايدار يون Al3+ يک مقدار نجومي و عظيم است! بنابراين اشتباه است که به دنبال يون Al4+ به عنوان محصول يک واکنش شيميايي باشيم.
برچسبها:
الکترون خواهي
همان گونه که مي دانيم، انرژي يونش، تمايل يک اتم خنثي براي مخالفت با از دست دادن الکترون را اندازه مي گيرد. يعني گرفتن يک الکترون از اتم، مستلزم صرف انرژي است (اين فرايند، گرماگير است). براي مثال، برداشتن يک الکترون از اتم فلوئور خنثي و تشکيل يون با بار مثبت، مقدار قابل ملاحظه اي انرژي لازم دارد:
F(g) F+(g) + e-  Ho = 1681.0 kJ/mol
Ho = 1681.0 kJ/mol
الکترون خواهي يک عنصر، مقدار انرژي خارج شده از آن است که در طول اين فرايند، يک اتم خنثي در فاز گازي، يک الکترون اضافي به دست مي آورد تا يون با بار منفي تشکيل دهد. براي مثال، زماني که اتم فلوئور در حالت گازي، الکترون به دست مي آورد تا يون منفي فلوئور تشکيل دهد، انرژي آزاد مي کند (تشکيل اين پيوند بين اتم فلوئور و الکترون خارجي، گرماده است):
F(g) + e-  F-(g)
F-(g)  Ho = -328.0 kJ/mol
Ho = -328.0 kJ/mol
اندازه گيري الکترون خواهي، مشکل تر از انرژي يونش است و معمولاً با ارقام با معني کم تري شناسايي مي شود. الکترون خواهي عناصر گروه هاي اصلي جدول تناوبي در شکل 1 نشان داده شده است. مي توان از اين شکل، اطلاعات زير را فهميد:
• به طور کلي، الکترون خواهي به دو دليل زير از بالا به پايين در هر ستون جدول تناوبي، کوچک تر مي شود؛ نخست، الکترون اضافه شده به اتم در اوربيتال هاي بزرگ تر جاي مي گيرد و زمان کم تري در اطراف هسته ي اتم صرف مي کند. دوم اين که تعداد الکترون هاي عناصر از بالا به پايين جدول تناوبي در هر ستون افزايش پيدا مي کند، بنابراين نيروي پس زني و دافعه بين الکترون اضافه شده و الکترون هاي موجود در اتم خنثي، بيش تر مي شود.
• به دليل اين که دافعه بين الکترون اضافه شده و الکترون هاي متعلق به اتم خنثي به حجم اتم بستگي دارد، داده هاي الکترون خواهي پيچيده تر مي شوند. در ميان نافلزات گروه هاي 6 و 7 اصلي، اين دافعه براي کوچک ترين اتم هاي دو ستون ياد شده (اکسيژن و فلوئور)، بزرگ ترين مقدار را دارد؛ بنابراين الکترون خواهي اين عناصر، کوچک تر از عناصر زيري آن ها در اين دو ستون است. اما به هر صورت، الکترون خواهي از بالا به پايين در حال کاهش است.
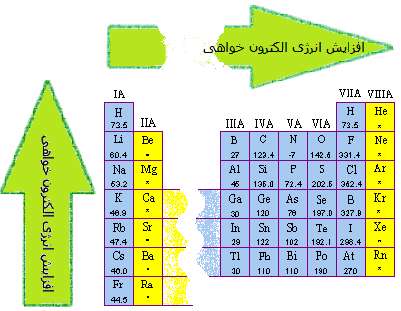
شکل 1: روندکلي تغييرات الکترون خواهي در جدول تناوبي
در داده هاي زير، هيچ الگوي خاصي در طول رديف هاي جدول تناوبي ديده نمي شود اما اين داده ها به همراه آرايش الکتروني اين عناصر، مفهوم پيدا مي کنند. در نتيجه، عناصري مانند هليوم، بريليوم، نيتروژن و نئون که آرايش الکتروني پايدار دارند، کشش کمي براي جذب الکترون اضافي دارند و زماني که اتم خنثي اين عناصر، الکترون اضافي به دست مي آورد، هيچ انرژي از خود آزاد نمي کنند.
آرايش اين عناصر چنان پايدار است که وادار کردن آن ها براي به دست آوردن الکترون اضافي و تشکيل يون منفي، واقعاً انرژي مي گيرد.
آرايش الکتروني و الکترون خواهي ده عنصر ابتدايي جدول تناوبي به همراه شکل آن ها.
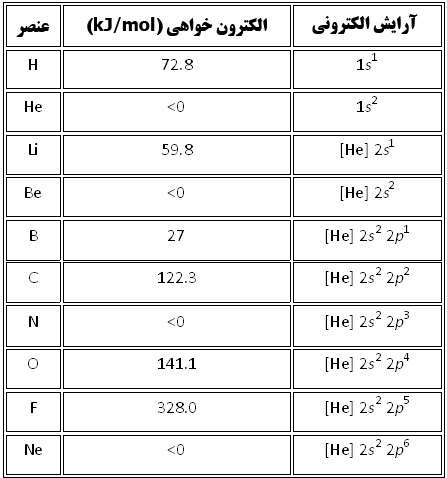
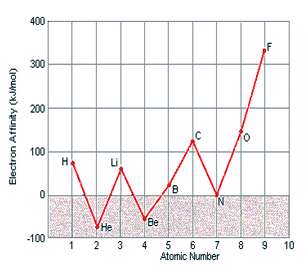
نتايج اندازه ي نسبي الکترون خواهي و انرژي يونش
اغلب تصور مي شود که سديم با کلر واکنش مي دهد تا يون هاي Na+ و Cl- تشکيل دهند زيرا اتم هاي کلر بيش تر از اتم هاي سديم، الکترو ن ها را "دوست دارند". شکي نيست که سديم به شدت با کلر واکنش مي دهد تا NaCl تشکيل دهد:
2 Na(s) + Cl2(g)  2 NaCl(s)
2 NaCl(s)
از اين گذشته، راحت حل شدن NaCl در آب که باعث هدايت الکتريسيته مي شود، گواه اين واقعيت است که محصول اين واکنش، يک نمک است و شامل يون هاي Na+ و Cl- است:
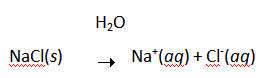
تنها سؤال مطرح شده در اين قسمت، اين است که آيا فرض الکترون دوست بودن اتم هاي کلر نسبت به اتم هاي سديم، جايز است؟
اولين انرژي يونش سديم 5/1 برابر بزرگ تر از الکترون خواهي کلر است:

بنابراين، برداشتن الکترون از اتم سديم خنثي، از الکترون به دست آوردن اتم کلر خنثي انرژي بيش تري مي گيرد و از اين خصلت کلر تأمين مي شود.
برچسبها:
ميدان مغناطيسي حاصل از سيملوله حامل جريان
سيم لوله از چند دور سيم تشكيل شده و شبيه فنر است. اگر جريان الكتريكي از سيم لوله عبور كند در اطراف سيم لوله خاصيت مغناطيسي ايجاد مي شود.

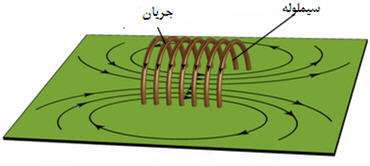
در شکل زير خطوط ميدان مغناطيسي ناشي از سيملوله نشان داده شده است اين خطوط داراي چه ويژگي هايي است؟
• خطوط ميدان در داخل سيملوله بسيار متراکم تر از خارج آن است.
• ميدان در داخل سيملوله به صورت خطوط موازي با فاصله هاي برابر رسم است كه نشان دهنده ميدان مغناطيسي يكنواخت در داخل سيم لوله مي باشد
جهت ميدان سيملوله
جهت ميدان در داخل سيملوله خلاف جهت ميدان در خارج آن است. جهت ميدان مغناطيسي طبق قانون دست راست در داخل سيملوله از S به N و در خارج سيملوله از N به S است. اگر انگشت شست دست راست در جهت جريان قرار گيرد بسته شدن چهار انگشت جهت ميدان را نشان مي دهد.
در شکل زير جهت خطوط ميدان مغناطيسي سيملوله نشان داده شده است:
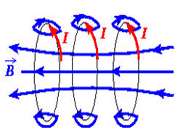
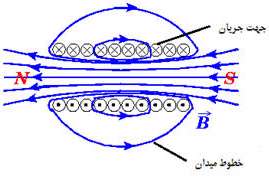
نکته:
سيملوله حامل جريان را مي توان همانند آهنرباي ميله اي فرض كرد، زيرا همان طور كه خطوط ميدان مغناطيسي يك سيملوله نشان مي دهد. همانند خطوط ميدان مغناطيسي آهنربا مي باشد يعني مي توان دو قطب N (انتهايي از سيملوله كه خطوط از ان خارج مي شود) و S ( انتهايي از سيموله كه خطوط به ان وارد مي شود) را در نظر گرفت 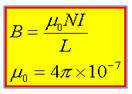
بزرگي ميدان در سيملوله از رابطه زير به دست مي آيد:
L : طول ميله I : شدت جريان N : تعداد حلقه
برچسبها:
قانون بقاي جرم لاوازيه
مقدمه

آزمايش هاي آنتوان لاوازيه، شروع يک انقلاب در علم شيمي است. اين آزمايش ها را مي توان سرآغاز علم شيمي جديد دانست. او با توجه به نتايج آزمايش هاي کمي به توضيح پديده هاي شيميايي دست يافت و نظريه فلوژيستون را در توجيه فرايندهاي شيميايي برانداخت.
قانون بقاي جرم
قانون بقاي جرم مي گويد که در جريان يک واکنش شيميايي تغييري در جرم ، که قابل تشخيص باشد روي نمي دهد.
تا قبل از قرن هجدهم ميلادي اصل بقاي جرم و اصل بقاي انرژي، دو اصل کلي و مستقل بودند که پايه هاي دانش را تشکيل مي دادند.
در نيمه دوم قرن هجدهم ميلادي لاوازيه دانشمند فرانسوي پس از يك سلسله تجربيات دريافت كه مقدار جرم ماده كه در فعل و انفعالات شيميايي دخالت دارند همواره ثابت مي ماند و اين مشخصه مواد رادر قانون زير به نام قانون بقاي جرم خلاصه نمود.
در محدوده فيزيک کلاسيک؛ در دستگاه هاي منزوي هيچ جرمي از بين نمي رود و هيچ جرمي نيز به خودي خود و بدون جرم ديگر به وجود نمي آيد و يا به عبارت ديگر مقدار جرم مادي كه در عالم وجود دارد همواره ثابت است. اصل بقاي انرژي مي گويد انرژي هر دستگاه معين مقدار ثابتي دارد. نه مي توان انرژي را خلق كرد و نه آن را از بين برد فقط انرژي از شکلي به شکل ديگر تغيير مي کند .
با وجود تغييراتي كه ممكن است در ديگر كميت هاي دستگاه (مثل انرژي ،حجم ودما ) رخ دهد، جرم كل دستگاه به شرط منزوي بودن ثابت خواهد بود. يعني اين كه جرم نمي تواند آفريده شود و يا از بين برود، يا توليد و يا نابود شود. به عبارت ديگر مي توان گفت كه جرم خاصيت زوال ناپذير ماده است كه در تغييرات شيميايي ماده همواره ثابت مي ماند. تنها از ماده اي به ماده ديگر منتقل مي شود به طور كلي در هيچ تغييري جرم ماده از بين نمي رود و يا به وجود نمي آيد. به طوري كه جرم كل جهان همواره ثابت مي ماند.

البته سيستم هايي وجود دارند كه جرم آن ها درطول زمان تغيير مي كند. به عنوان مثال اگر حركت موشك را در نظر بگيريم. موشك قبل از پرتاب داراي يك مقدار جرم كل خواهد بود . اما بعد از پرتاب سوخت موشك مصرف مي شود بنابراين جرم سيستم موشك در اين لحظه با جرم آن قبل از پرتاب متفاوت خواهد بود. پس سيستم بقا نخواهد داشت. با اين حال اگر موشك و گازهاي خارج شده از آن را كلا به صورت يك سيستم فرض كنيم در اين صورت نيروهايي كه گازها ي خارج شده و موشك به يكديگر وارد مي كنند، در حكم نيروهاي داخلي بوده و شرط منزوي بودن سيستم برقرار مي شود و باز جرم بقا خواهد داشت.
درحالتي كه سرعت جسم نزديك به سرعت نورباشد، دراين صورت ديگر در قلمرو فيزيك كلاسيك نخواهيم بود و لذا قانون بقاي جرم نقض مي شود .
قانون بقاي جرم - انرژي: گفتيم كه اگر سرعت جسمي بتواند نزديك به سرعت نور برسد، در اين صورت از محدوده فيزيك كلاسيك خارج خواهيم شد. در اين حالت قوانين بقاي جرم وانرژي نقض مي شود، ودر عوض يك قانون واحد به نام قانون بقاي جرم- انرژي بيان مي شود. براين اساس هرگاه تغييري در مقدار جرم صورت گيرد، اين تغيير به وسيله تغيير انرژي جبران مي شود.
به عنوان مثال اگر جرم كاهش يابد، در اين صورت به اندازه تغيير جرم انرژي توليد مي شود و برعكس، اگرجرم افزايش يابد، مقداري انرژي به جرم تبديل شده است. هم ارزي بين جرم و انرژي اولين بار توسط اينشتن در نظريه نسبيت بيان شد. در مورد تبديلات هسته اي نيز هم ارزي بين جرم وانرژي حاکم است.

لاوازيه اعلام کرد که تغييرات انرژي در واکنش هاي شيميايي معمولي ممکن است در نتيجه تغيير جرم باشد ولي اين گونه تغييرات جرمي بسيار کمتر از آن است که از طريق آزمايش قابل تشخيص باشد ازاين رو قانون بقاي جرم همان طوري که بيان شد ، براي تمام واکنش ها معتبر است به استثناء واکنش هايي که با تغييرات هسته اي همراه باشند
. اين قانون نخستين بار توسط آنتوان لاوازيه در اثري از او با عنوان بررسي مقدماتي شيمي 1 رسماً بيان شده است ولي کساني هم که پيش از او با روش هاي کمي سروکار داشته اند چنين اصلي را پذيرفته بودند قانون بقاي جرم تا آنجا که به معادلات شيميايي مربوط مي شود به اين معني است که اتم هاي هر عنصر خواه ترکيب شده وخواه ترکيب نشده به همان تعداد که در طرف چپ معادله ديده مي شوند در طرف راست آن هم بايد وجود داشته باشند.
برچسبها:
پيوندهاي شيميايي
مي دانيم اتم ها اجزاي سازنده ي تمام مواد هستند و از طريق پيوندهاي شيميايي ناشي از نيروهاي جاذبه ي قوي که بين آن ها وجود دارد، به هم ديگر اتصال پيدا مي کنند. اما دقيقاً يک پيوند شيميايي چيست؟
ناحيه اي که هنگام برهم کنش الکترون هاي اتم هاي مختلف با يکديگر ايجاد مي شود، پيوند شيميايي ناميده مي شود. الکترون هايي که در پيوند شيميايي شرکت مي کنند، الکترون هاي ظرفيت ناميده مي شوند که در خارجي ترين پوسته اتم يافت مي شوند.
زماني که دو اتم به هم ديگر نزديک مي شوند، الکترون هاي خارجي ترين لايه ي هر دو با هم اندرکنش مي کنند. با اين که الکترون ها هم ديگر را دفع مي کنند،اما باعث جذب پروتون هاي درون اتم مقابل خود مي شوند. اثر متقابل نيروها در اتم ها باعث تشکيل پيوند بين آن ها و اتصالشان به هم ديگر خواهد شد.
همان گونه که از اطلاعات اوليه ي شيمي مي دانيم، عناصر گازي بي اثر گروه 8 به صورت گازهاي تک اتمي وجود دارند و در حالت کلي با ديگر عناصر واکنش نمي دهند. در مقابل، ديگر عناصر گازي به صورت مولکول هاي دو اتمي وجود دارند (H2, N2, O2, F2, Cl2) و همگي به جز نيتروژن، واکنش پذير هستند. واکنش پذيري اين عناصر در معادلات زير نشان داده شده است:
2Na + Cl2 ........ 2NaCl
2H2 + O2 ......... 2H2O
C + O2 .......... CO2
C + 2F2 .......... CF4
اکنون سؤال اين است که چرا اتم هاي بسياري از عناصر با هم واکنش نشان مي دهند تا مولکول هاي پايداري به وجود آورند؟
براي پاسخ به اين سؤال، ابتدا بهتر است با يک مدل بسيار ساده براي جذب يا پيوند اتم ها به يکديگر شروع کنيم و سپس به توضيحات سطح بالا برسيم.
دو نوع اصلي پيوند بين اتم ها، پيوند يوني و کوالانسي است. اما انواع ديگر پيوند هم وجود دارد.
پيوند يوني:
يک پيوند يوني زماني تشکيل مي شود که اتمي، يک يا چند الکترون ظرفيت خود را به اتم ديگري ببخشد يا همين الکترون ها را از اين اتم بپذيرد.
به عنوان مثال، زماني که سديم در محيطي که داراي گاز کلر است، سوزانده شود، ترکيب سديم کلرايد توليد مي کند(معادله ي اول). اين ترکيب، نقطه ي ذوب بالايي دارد (800° C) و در آب حل مي شود تا يک محلول رسانا حاصل کند.
سديم کلرايد يک ترکيب يوني است. در شکل 1 (الف و ب)،تشکيل پيوند سديم کلرايد و نوع پيوند آن ها را مشاهده مي کنيد. ساختار جامد کريستالي سديم کلرايد به صورت ج است.
 (ب)
|
(الف) |
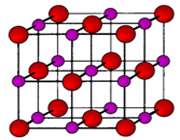
(ج)
شکل 1: پيوند يوني سديم کلرايد.
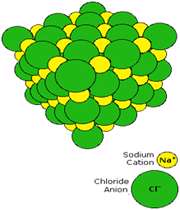
انتقال تنها الکترون 3s اتم سديم به اوربيتال نيمه پر 3p اتم کلر، کاتيون سديم (لايه ي ظرفيت اين يون مثبت،مانند آرايش نئون است) و آنيون کلر (لايه ي ظرفيت اين يون منفي،مانند آرايش آرگون است) توليد مي کند. جاذبه ي الکتروستاتيکي منجر مي شود يون هاي با بارمخالف در يک شبکه ي بلوري (شکل 1- ج) به هم فشرده شده و روي هم انباشته شوند (شکل 2).
نيروهاي جاذبه اي که اين يون ها را در محل خود، متصل به هم نگه مي دارند، مي توانند به عنوان پيوند هاي يوني شناخته شوند.
شکل 2: انباشتگي يون هاي منفي و مثبت کلر و سديم در سديم کلرايد.
پيوند کوالانسي:
در 3 واکنش ديگر معادلات بالا، محصولاتي توليد مي شود که بسيار متفاوت با سديم کلرايد هستند. آب در دماي اتاق، مايع است و دي اکسيدکربن و تترافلوئوريد کربن،گاز هستند. اين ترکيبات از يون تشکيل نشده اند.
يک اندرکنش متفاوت بين اتم ها، پيوند کوالانسي ناميده مي شود که با اشتراک الکترون هاي والانس (ظرفيت) اتم ها به جاي انتقال آشکار الکترون در پيوند يوني، اتفاق مي افتد. شباهت هاي خواص فيزيکي عناصر دو اتمي H2، N2، O2، F2 و Cl2 (همگي به صورت گاز هستند) پيشنهاد مي کند که پيوند کوالانسي هم داشته باشند.
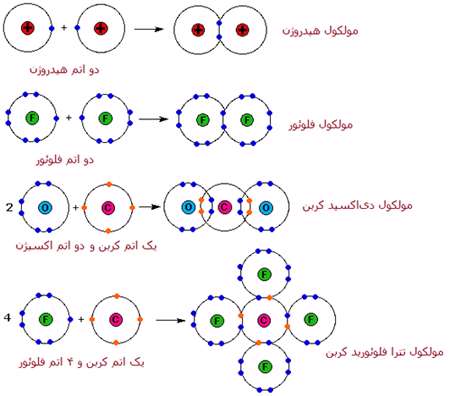
انواع پيوندهاي کوالانسي معادلات بالا
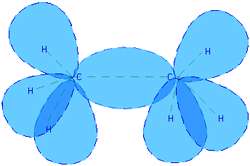
شکل 3: پيوند کوالانسي در مولکول اتان.
لازمه ي پيوند کوالانسي اين است که ترازهاي انرژي يا لايه هاي بيروني تر اتم ها به طور کامل پر نشده باشند تا الکترون هاي اين اتم ها کاملاً بين آن ها به اشتراک گذاشته شوند. در الماس، اتم هاي کربن پيوندهاي کوالانسي با يکديگر تشکيل مي دهند. پيوند کوالانسي، پيوندي بسيار قوي است.
پيوند کوالانسي قطبي:
اين پيوندها بين پيوندهاي يوني و کوالانسي قرار مي گيرند. در اين پيوند، اتم ها الکترون هايشان را به اشتراک مي گذارند اما الکترون ها بيش تر وقت خود را در اطراف اتمي با مقدار الکترونگاتيوي بزرگ تر مي گذرانند. بهترين مثال اين پيوند،
مولکول آب است. اکسيژن بسيار الکترونگاتيوتر از هيدروژن است؛ بنابراين الکترون هاي شرکت کننده در پيوند قطبي آب، بيش تر وقت خود را سمت اکسيژن سپري مي کنند.
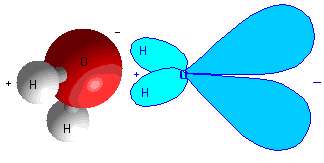
شکل 4: مولکول قطبي آب.
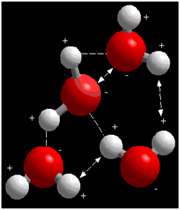 پيوند هيدروژني:
پيوند هيدروژني:

در مولکول آب، اين موضوع که اکسيژن به طور منفي و هيدروژن به طور مثبت باردار شده، به اين معناست که هيدروژن هاي يک مولکول آب، اکسيژن هاي همسايه ي خود را جذب مي کنند و برعکس.
زيرا بار هر دو مخالف هم است. اين جاذبه ي بزرگ الکتروستاتيکي، پيوند هيدروژني ناميده مي شود و در تعيين بسياري از خواص آب نقش دارد. مولکول آب مي تواند اين نوع پيوند را با مولکول هاي قطبي يا يون هاي ديگري مانند هيدروژن يا سديم تشکيل دهد.
علاوه بر اين، پيوندهاي هيدروژني مي توانند درون و بين ديگر مولکول ها نيز اتفاق بيفتند. براي مثال، دو رشته مولکول DNA با پيوند هيدروژني به هم ديگر اتصال پيدا مي کنند.
شکل فوق، گروه کوچکي از مولکول هاي آب را نشان مي دهد. پيوندهاي هيدروژني بين بارهاي مخالف با خط تيره نشان داده شده اند. خطوط پيکان دار دافعه ي بين بارهاي مشابه را نشان مي دهند. تعادل پيوندهاي هيدروژني و نيروهاي دافعه در خواص ويژه ي آب نقش مهمي دارند.
پيوند ديگري که ممکن است وجود داشته باشد، پيوند فلزي است. زماني که الکترون هاي دو اتم فلزي به اشتراک گذاشته شوند، پيوند فلزي تشکيل مي-شود.
برچسبها:
کارخانه برگ
ديد کلي
به طور کلي گياهان گياهان به طور مستقيم و غير مستقيم در زندگي انسان ها، مؤثر هستند. مثلاً با خوردن ميوه ها از آن ها تغذيه مي کنيم و يا از گوشت برخي از حيوان ها که از گياهان تغذيه مي کنند، استفاده مي کنند.
انرژي خورشيد تاثير بسيار زيادي بر زندگي روي کره زمين دارد. از اين انرژي، در فتوسنتز که تنها فرايند مهم بيولوژيکي است، استفاده مي شود.
تعريف فتوسنتز
تمام موجودات زنده از خورشيد انرژي مي گيرند، اما در ميان موجودات زنده فقط گياهان سبز ميتواند به صورت مستقيم اين انرژي را به کار گيرند و به کمک مواد اوليه ساده اي ، نظير دي اکسيد کربن ، آب و آمونياک ترکيبات ياخته اي به وجود آورند. اين فرايند نور ساخت يا فتوسنتز ناميده مي شود.
کاربرگ
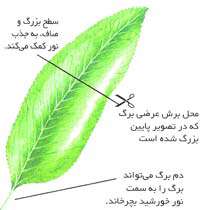
برگ هاي گياه، کارخانه هاي حيرت آوري هستند. آن ها به صورت خاصي با انجام بسياري از عملکردهاي گياه سازگاري يافته اند. مهم ترين اين عملکردها، فرايند غذاسازي(فتوسنتز)است. براي انجام اين فرايند، برگ بايد يک منطقه خوب داشته باشد. اين دستگاه، به آب و مواد معدني اجازه عبور به سمت برگ و به غذا اجازه حرکت به محل مورد نياز را مي دهد.
برگ ها سرعت دستگاه انتقال دهنده را کنترل کرده و آب از دست رفته را جبران مي کنند. برگ ها به کنترل دما در گياه نيز کمک مي کنند.
اگر بخواهيم به طور دقيق تر بيان کنيم؛ گياهان به چند چيز نياز دارند تا غذايشان را بسازند که عبارتند از:
کلروفيل که يک رنگدانه سبز است و در برگ هاي گياهانپيدا مي شود.
نور طبيعي خورشيد و يا نور مصنوعي، مثل نوري که که از لامپ مي آيد.
دي اکسيد کربن که در هوا يافت مي شود، اين گاز در بازدم انسان ها وجود دارد.
آب که از طريق ريشه ها جمع آوري مي شود.
مواد مغذي و معدني که از خاک توسط ريشه گياهان به گياهان مي رسد.
گياهان غذاي خود را در برگ هايشان مي سازند. برگ ها رنگدانه اي به نام کلروفيل دارند که باعث سبزي گياهان مي شود در گياهان کلروفيل با وجود تمام مواد مورد نياز براي تهيه غذا، غذاي گياهان را آماده مي کنند.
به شکل زير خوب دقت کنيد:
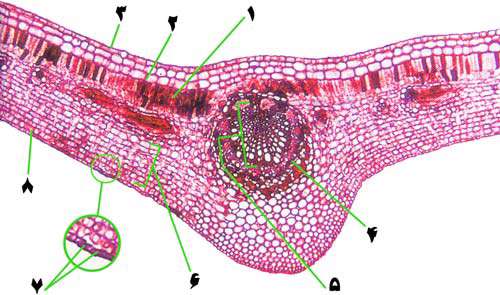
1- سلول هاي بافت پارانشيم، بيشترين مقدار کلروپلاست را دارند. بنابراين فتوسنتز در اين محل انجام مي شود. کلروپلاست ها مي توانند در سلول پخش شده يا براي جذب بيشتر يا کم تر نور خورشيد، به طور خطي رديف شوند.
2- لايه اپيدرمي
3- کتويکول لايه مومي و غير قابل نفوذي است که ازافزايش تعرق جلوگيري مي کند.
4- سلول هاي آوند آبکش و چوبي مجراهايي را مي سازند که به ترتيب شيره پرونده (غذاي آماده) و شيره خام (آب و مواد معدني) را عبور مي دهند. اين سلول ها، شيره پرورده را از برگ به همه جاي گياه و شيره خام را از ريشه به برگ انتقال مي دهند.
5- آوند چوبي
6- سلول هاي مزوفيل (ميان برگ) از بافت پارانشيمي درست شده که داراي کلروپلاست بوده و ماده غذايي در آن ها ساخته مي شود. اين براي آن که فضاي کافي بين آن ها وجود داشته و هوا به راحتي در بين آن ها جريان يابد، به صورت نامنظم کنار هم قرار گرفته اند.
اين وضعيت به ورود کربن دي اکسيد و خروج اکسيژن کمک مي کند.
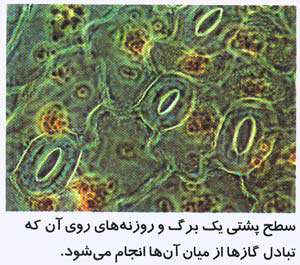
7- سلول هاي نگهبان روزنه اندازه روزنه ها را در برگ کنترل مي کنند. به اين ترتيب مقدار تعرق تنظيم مي شود.
8- لايه اپيدرم براي عبور نور و رسيدن آن به کلروپلاست قابليت ويژه انتقال را داراست.
درمورد مسائل زير فکر کنيد:
1- اکثر برگ ها، روزنه هايي در سطح زيرين خود دارند. فايده آن ها چيست؟
2- در اکثر برگ ها، کلروپلاست بيشتر در نيمه بالايي آن يافت مي شود، علت چيست؟
3- سلول هاي پارانشيم، استوانه اي شکل هستند. اين بدان معناست که فضاي بيشتري ميان آن ها وجود دارد. داشتن اين فضاهاي بين سلولي، چه مزيتي در بر دارد؟
4- انتظار داريد چه ويژگي هاي اختصاصي در اندام هاي گياهاني که در مناطق خيلي خشک زندگي مي کنند، وجود داشته باشد؟
5- انتظار داريد چه تفاوت هايي ميان گياهاني که برگ هايشان يه طور عمودي رشد مي کنند با ساير گياهان وجود داشته باشد؟
مکانيزم عمل فتوسنتز
حدود 2 درصد از نور خورشيد که بر گياه مي تابد، به انرژي شيميايي تبديل مي شود. هنگامي که نور بر گياه مي تابد، بيشترين مقادير انرژي توسط دانه هاي کوچکي مرسوم به کلروپلاست (Chloroplast) جذب مي شود. کلروفيل ها، انرژي نوراني را به انرژي شيميايي تبديل مي کنند و اين تبديل انرژي طي فرايند فوتوليز (Photolysis) تجزيه شيميايي بر اثر تابش) ، که در آن آب به کمک نور خورشيد تجزيه وآدنوزين تري فسفات فعال مي شود، صورت مي گيرد.

اين فرايند، به نوبه خود به عمل تثبيت دي اکسيد کربن (ممانعت از حالت فرار يا جامد شدن دي اکسيد کربن) انرژي مي دهد و تشکيل مولکول هاي قندو نشاسته را مقدور مي کند. از تجزيه آب به هيدروژن آزاد، در جو اوليه زمين وجود نداشت، بنابراين، کل دستگاه تنفسي ما به طور کامل تابع اين بود که بر اثر عمل نور ساخت روي زمين و در دريا، چه چيزي توليد مي شود. در مرحله بعدي فتوسنتز ، دي اکسيد کربن به انضمام چهار اتم هيدروژن، قند و آب تشکيل مي شود. اين فرايند سرآغاز حرکتي است پيچيده تر و کارآمدتر.
برچسبها:
فشار اسمزي
در ابتدا با مفاهيم زير آشنا مي شويم :
- غشاي نيمه تراوا : غشايي که نسبت به بعضي از اجزاي محلول نفوذ پذير و نسبت به سايرين غير نفوذ پذير است. مثل غشاهاي سلولي و سلوفان.
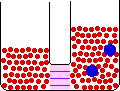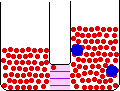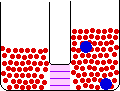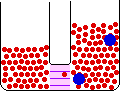
- اسمز : حرکت اجزاء از محلولي با غلظت بيشتر به طرف محلولي با غلظت کم تر.
اين حرکت براي حلال اين گونه توجيه مي شود: حرکت حلال از محلولي با غلظت حل شونده ي کم تر به سمت محلولي حاوي غلظت حل شونده ي بيشتر.

- محلول ايزوتونيک : محلولي با فشار اسمزي يکسان در دو طرف يک غشاي نيمه تراوا.
- محلول هيپوتونيک : محلولي با فشار اسمزي اي کم تر از محلول هيپرتونيک که داراي فشار اسمزي بالايي است.
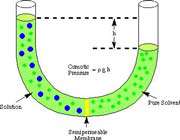
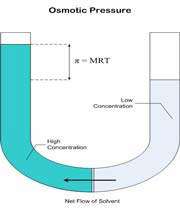
اگر لوله ي U شکل زير را در نظر بگيريد:
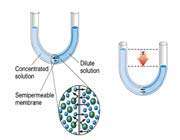
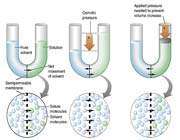
حلال از بازوي سمت راست که داراي محلول رقيق است ( غلظت حلال بيشتر است ) به طرف محلول غليظ ( محلول شامل آب و نمک ) واقع در بازوي سمت چپ، از طريق غشاي نيمه تراوا در حال حرکت است. بنابراين رفته رفته مقدار آب در بازوي سمت چپ افزايش مي يابد و محلول رقيق تر مي گردد و سطح مايع در لوله بالاتر مي رود. در اين جا اختلاف فشار به صورت اختلاف ارتفاع در دو سمت بازو ايجاد مي شود که به صورت فشار در شکل ظاهر شده است. اين فشار را فشار اسمزي مي نامند.
فشار اسمزي به صورت زير توسط جاکوب وانت هوف ( Jacobus Henricus van"t Hoff ) فرمول بندي شده است:

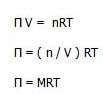
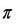 نشان دهنده ي فشار اسمزي، R ثابت گاز ايده آل، M مولاريته ي محلول بر حسب مول در ليتر و T دما را بر حسب کلوين نشان مي دهد.
نشان دهنده ي فشار اسمزي، R ثابت گاز ايده آل، M مولاريته ي محلول بر حسب مول در ليتر و T دما را بر حسب کلوين نشان مي دهد.
ماهيت فشار اسمزي
غشايي مانند سلوفان که برخي از مولکول ها ، نه همه آنها ، را از خود عبور ميدهد، غشاي نيمه تراوا ناميده ميشود. غشايي را در نظر ميگيريم که بين آب خالص و محلول قند قرار گرفته است. اين غشا نسبت به آب ، تراوا است، ولي «ساکارز» (قند نيشکر) را از خود عبور نميدهد. در شروع آزمايش ارتفاع آب در بازوي چپ لوله U شکل برابر با ارتفاع محلول قند در بازوي راست اين لوله است. از اين غشا ، محلول هاي قند نميتوانند عبور کنند، ولي مولکول هاي آب در هر دو جهت ميتوانند عبور کنند.
در بازوي چپ لوله فوق (بازويي که محتوي آب خالص است)، تعداد مولکول هاي آب در واحد حجم بيش از تعداد آنها در بازوي راست است. از اينرو ، سرعت عبور مولکول هاي آب از سمت چپ غشا به سمت راست آن بيشتر از سرعت عبور آنها در جهت مخالف است. در نتيجه ، تعداد مولکول هاي آب در سمت راست غشا به تدريج زياد ميشود و محلول قند رقيقتر ميگردد و ارتفاع محلول در بازوي راست لوله U زياد ميشود. اين فرايند را اسمز مينامند.
اختلاف ارتفاع در سطح مايع در دو بازوي لوله U ، اندازه فشار اسمزي را نشان ميدهد. بر اثر افزايش فشار هيدروستاتيکي در بازوي راست که از افزايش مقدار محلول در اين بازو ناشي ميشود، مولکول هاي آب از سمت راست غشا به سمت جپ آن رانده ميشوند تا اينکه سرانجام سرعت عبور از سمت راست با سرعت عبور از سمت چپ برابر گردد.
بنابراين حالت نهايي يک حالت تعادلي است که در آن ، سرعت عبور مولکولهاي آب از غشا در دو جهت برابر است.
پديده ي اسمز در گلبول هاي قرمز بدن نيز وجود دارد. به اين صورت که اگر گلبول هاي قرمز خون را در محلول آب خالص قرار دهيم، مولکول هاي آب از جداره ي نيمه تراواي گلبول قرمز عبور کرده و به درون گلبول قرمز راه مي يابند. غلظت حلال آب که در اطراف سلول خوني بيشتر بوده و حال به درون سلول خوني راه يافته اند، در نتيجه مقدار آب درون گلبول رفته رفته افزايش يافته و منجر به پاره شدن جداره ي سلول خوني مي شود.
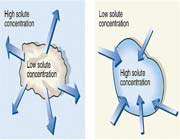
اما اگر همين گلبول در محيط آب و نمک قرار گيرد، چون داراي حلال بيشتري است آب از گلبول به محيط اطراف نفوذ مي کند و در نتيجه منجر به چروکيده شدن گلبول مي شود. بنابراين در تزريقات وريدي بايستي از محلول هايي ( ايزوتونيک )استفاده شود که داراي فشار اسمزي يکسان با فشار اسمزي خون باشند.
زماني که در لوله ي U شکل، آب از غشاي نيمه تراوا عبور مي کند و فشار اسمزي را ايجاد مي سازد، به علت فشار هيدروستاتيکي محلولي که داراي غلظت حلال بيشتري است، آب مجددا از همان بازو به بازوي ديگري در لوله ي U شکل جريان مي يابد تا زماني که سرعت عبور آب در دو طرف غشا برابر شود در نتيجه فشار تعادلي نيز برقرار مي گردد.
حال اگر فشاري بيشتر از فشار تعادلي بر روي بازوي شامل حلال و ماده ي حل شده وارد گردد، حلال آب مجددا از همان بازو به بازوي ديگري جريان مي يابد و پديده ي اسمز معکوس صورت مي گيرد.
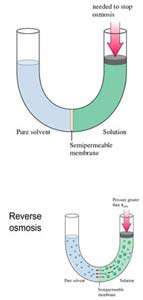
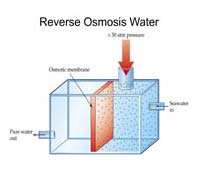
از روش اسمز معکوس براي خالص سازي آب دريا نيز استفاه مي شود.
برچسبها:







 آمار
وب سایت:
آمار
وب سایت:

