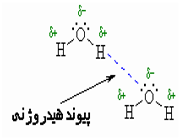
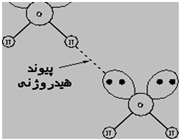
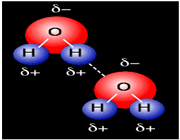
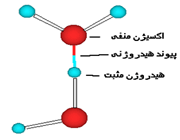
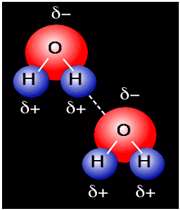
پیوند هیدروژنی
جاذبه بین مولکولی دربرخی از ترکیبات هیدروژندار به طور غیرعادی قوی است این جاذبه در ترکیباتی مشاهده میشود که درآن ها بین هیدروژن و عناصری که اندازه کوچک و الکترونگاتیوی زیاد دارند پیوند هیدروژنی وجود دارد. پیوند هیدروژنی نه تنها بین مولکول های یک نوع ماده، بلکه بین مولکول های دو ماده متفاوت که توانایی تشکیل پیوند هیدروژنی را دارند نیز برقرار میشود.
تعریف پیوند هیدروژنی Hydrogen Bond
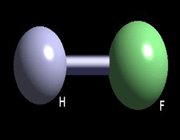
هرگاه هیدروژن به اتمی با الکترونگاتیوی زیاد مثل فلوئور، اکسیژن یا نیتروژن متصل گردد، شرایطی برای به وجود آمدن نوع بسیاری مهمی جاذبه بین مولکولی مثبت ـ منفی حاصل میشودکه به آن پیوند هیدروژنی میگویند.
به عبارت دیگر، اتم یک مولکول هیدروژن و زوج الکترون غیر مشترک مولکول دیگر متقابلا همدیگر را جذب میکنند و پیوندی تشکیل میشود که به پیوند هیدروژنی مرسوم است.
نحوه تشکیل پیوند هیدروژنی
پیوند هیدروژنی بر اثر جاذبه اتم هیدروژن اندک مثبت موجود در یک مولکول و اتم بسیار الکترونگاتیو موجود در مولکول دیگر (یا در محل دیگر همان مولکول اگر مولکول به قدر کافی بزرگ باشد که بتواند روی خود خم شود) تولید میگردد.
جا به جا شدن یک جفت الکترون به سمت عنصر بسیار الکترونگاتیو نیتروژن، اکسیژن یا فلوئور باعث میشود که این اتم ها دارای بار منفی جزئی شوند. در این صورت پیوند هیدروژنی پلی است میان دو اتم شدیدا الکترونگاتیو با یک اتم هیدروژن که از طرفی به طور کوالانسی با یکی از اتم های الکترونگاتیو و از طرف دیگر بطور الکترواستاتیکی (جاذبه مثبت به منفی) با اتم الکترونگاتیو دیگر پیوند یافته است.
استحکام پیوند هیدروژنی یک دهم تا یک پنجاهم قدرت یک پیوند کوالانسی متوسط است.
شرایط تشکیل پیوند هیدروژنی
1. بالا بودن الکترونگاتیوی اتم های متصل به هیدروژن
برهمین اساس است که فلوئور (الکترونگاتیوترین عنصر) قویترین پیوند هیدروژنی را تشکیل می دهد و اکسیژن (الکترونگاتیوتر از نیتروژن) پیوند هیدروژنی قویتری درمقایسه با نیتروژن تشکیل میدهد.
هم چنین بار مثبت زیاد بر روی اتم هیدروژن، زوج الکترون مولکول دیگر را به شدت جذب میکند و کوچک بودن اندازه اتم هیدروژن سبب میشود که ملکول دوم بتواند به آن نزدیک شود.
2. کوچک بودن اتم های متصل به هیدروژن
پیوند هیدروژنی واقعا مۆثر فقط در ترکیبات فلوئور، اکسیژن و نیتروژن تشکیل میشود. با وجود این که دو اتم نیتروژن و کلر الکترونگاتیوی برابر دارند چون اتم کلر از اتم نیتروژن بزرگ تر است بر خلاف نیتروژن، کلر پیوند هیدروژنی ضعیفی تشکیل میدهد.
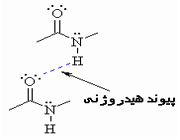
توجیه خواص غیرعادی برخی از مواد
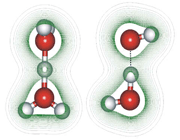
وجود خواص غیرعادی برخی از مواد در حالت جامد یا مایع از جمله بالا بودن دماهای ذوب و جوش، نشان میدهد که نیروهای جاذبه بین مولکولی در آن ها به اندازهای زیاد است که نمیتوان آن را به تأثیرهای متقابل ضعیف بین مولکولی نسبت داد. آشناترین این نوع مواد فلوئورید هیدروژن، آب و آمونیاک است که بسیاری از خواص آن ها از جمله دماهای جوش و ذوب آن ها از دماهای جوش و ذوب ترکیب های مشابه خود به طور غیرمنتظرهای بالاتر است.
شاید تصور شود که علت این وضعیت غیر عادی، قطبیت به نسبت زیاد این مولکول هاست؛ البته تا اندازهای همین طور است، اما بررسی دقیق این پدیده غیر عادی نشان میدهد که باید نیروی جاذبه قوی تر از نیروهای جاذبه دوقطبی _ دوقطبی بین مولکول های آن ها برقرار باشد.
اگر به ساختار الکترونی مولکولی آن ها توجه شود، میتوان به موردهای مشترک بین آن ها پی برد:
این وجه اشتراک، وجود دست کم یک پیوند کوالانسی با اتم هیدروژن و یک اوربیتال هیبریدی ناپیوندی دو الکترونی اتم مرکزی بسیار الکترونگاتیو در هر یک از آن هاست
اتم هایی که الکترونگاتیوی بالایی دارند با هیدروژن پیوند کوالانسی به شدت قطبی به وجود میآورند به طوری که هیدروژن به میزان قابل توجهی خصلت یک پروتون را پیدا میکند.
جفت الکترون ناپیوندی و قابل واگذاری روی اتم H، این امکان را پدید میآورد که اتم هیدروژن در نقش پل، اتمهای الکترونگاتیو دو مولکول را به یکدیگر متصل کند و نیروی جاذبه بین مولکولی بوجود میآید که به پیوند هیدروژنی مرسوم است.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
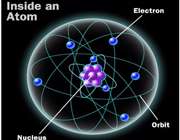
ساختار اتم
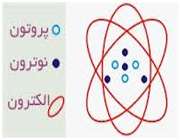
در آزمایش ها نیز مشخص گردید که اتم ها نیز خود از ذرات کوچک تری ساخته شده اند. در مرکز یک هسته کوچک مرکزی مثبت متشکل از ذرات هسته ( پروتون ها و نوترون ها) و بقیه اتم فقط از پوسته های متموج الکترون تشکیل شده است. معمولا اتم های با تعداد مساوی الکترون و پروتون، از نظر الکتریکی خنثی هستند.
ذرات سازنده اتم
الکترون: دارای بار منفی و جرم ناچیز است و به دور هسته می چرخند
پروتون: دارای بار مثبت و جرمی معادل 1840 برابر الکترون و تعیین کننده نوع اتم نوترون: بدون بار الکتریکی (خنثی) با جرمی معادل جرم پروتون
عدد اتمی (Z)
به تعداد پروتون های هر اتم(به تعداد بارهای مثبت اتم) عدد اتمی می گویند برای مثال اتم سدیم 11 پروتون دارد, پس عدد اتمی سدیم 11 است. عدد اتمی را گوشه پایین سمت چپ نماد شیمیایی می نویسند 11Na
عدد جرمی (A)
به مجموع تعداد پروتون ها و نوترون های یك اتم عدد جرمی گفته می شود.
تمام اتم های یك عنصر پروتون های یكسان دارند اما تعداد نوترون های آن ها می تواند متفاوت باشد.
عدد جرمی در گوشه بالا و سمت چپ نماد شیمیایی نوشته می شود مثلا اتم كربن در هسته خود 6 پروتون و 6 نوترون دارد پس عدد جرمی آن 12 است. 12C
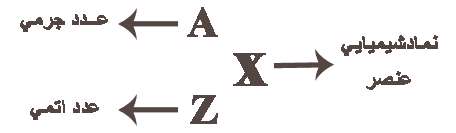
شیمیدان ها برای بیان جرم عنصرها بدین صورت عمل کردند که: فراوان ترین ایزوتوپ کربن یعنی کربن 12 را به عنوان استاندارد انتخاب کردند و جرم عنصرهای دیگر را با استفاده از نسبت هایی که در محاسبات آزمایشگاهی بدست آمده بود، بیان کردند.
به عنوان مثال جرم اتم اکسیژن 33/1 برابر جرم اتم کربن است. با توجه به این که جرم اتم کربن 12 می باشد جرم اتم اکسیژن را محاسبه کرد. در این مقیاس جرم اتم اکسیژن برابر 16خواهد شد.
واحد جرم اتمی amu است که کوتاه شده ی عبارت atomic mass unitاست. در این مقیاس جرم پروتون و نوترون lamu است.
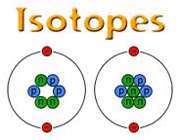
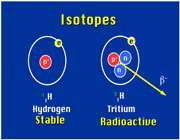
ایزوتوپ
ایزوتوپ ها، اتم های یك عنصر هستند كه در تعداد نوترون و در نتیجه عدد جرمی با هم تفاوت دارند اما عدد اتمی آن ها یكسان است.
مثلا هیدروژن دارای سه ایزوپ است.

بیشتر عناصر، یك ایزوتوپ معمول و چند ایزوتوپ كمیاب دارند به ایزوتوپ های كمیاب تر ناخالصی های ایزوتوپی می گویند.
مثلا ایزوتوپ معمول ئیدروژن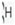 است كه 9/99 درصد كل هیدروژن های موجود در طبیعت را شامل می شود. كم تر از 1/0 درصد را
است كه 9/99 درصد كل هیدروژن های موجود در طبیعت را شامل می شود. كم تر از 1/0 درصد را 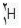 و مقدار ناچیزی را
و مقدار ناچیزی را 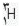 شامل می شود.
شامل می شود.

هنگامی که به وسیله اتم، یک یا چند الکترون از یک اتم دیگر جدا می گردد، یون ها ایجاد می شوند. یون ها اتم هایی هستند که به علت عدم تساوی تعداد پروتو ن ها و الکترون ها، دارای بار الکتریکی ویژه می شوند. یون هایی که الکترون(ها) را بر می دارند، آنیون (anion) نامیده شده و بار منفی دارند.
اتمی که الکترون(ها) را از دست می دهد کاتیون (cation) نامیده شده و بار مثبت دارد. کاتیون ها و آنیون ها به علت نیروی کولمبیک(coulombic) میان بارهای مثبت و منفی، یکدیگر را جذب می نمایند.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
اوربیتال اتمی
از نظر لغوی اوربیتال به معنای خانه الکترون میباشد و ناحیهای است که احتمال یافتن الکترون در آن زیاد است. معادله شرودینگر پایه مکانیک موجی است. این معادله بر حسب یک تابع موجی سای برای الکترون نوشته میشود. از حل معادله شرودینگر اتم هیدروژن یک سلسله جواب به عنوان تابع موج بدست میآید. تابع موج ناحیهای در اطراف هسته را نشان میدهد که در آن ناحیه، احتمال یافتن الکترون وجود دارد.
اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیش ترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
هر الکترون را میتوان با چهار عدد کوانتومی مشخص کرد که به منزله شناسنامه الکترون هستند و فاصله نسبی الکترون از هسته (n)، لایه فرعی و شکل اوربیتال (L) ، جهت گیری اوربیتال در فضا (s) را بیان میکنند.
تفسیر مکانیکی اوربیتال
شدت هر موج با مجذور دامنه آن متناسب است. تابع موجی (سای) ، تابع دامنه است. مجذور دامنه یا مجذور تابع موجی برای یک حجم کوچک در هر موقعیتی از فضا با چگالی بار الکترونی در آن حجم متناسب است.
میتوان تصور کرد که بار الکترونی به سبب حرکت سریع الکترون به صورت ابر باردار در فضای دور هسته گسترده شده است. این ابر در برخی نواحی غلیظ تر از برخی نواحی دیگر است. احتمال یافتن الکترون در هر ناحیه معین متناسب با چگالی ابر الکترونی در آن ناحیه است. این احتمال در ناحیهای که ابر الکترونی غلیظ تر باشد، بیشتر خواهد بود.
این تفسیر کوششی برای توصیف مسیر الکترون به عمل نمی آورد، بلکه فقط پیشبینی میکند که احتمال یافتن الکترون در کجا بیشتر است. از نظر مکانیک کوانتومی هیچ محدودیتی برای وجود الکترون در فضا اطراف هسته وجود ندارد. پس بینهایت اوربیتال وجود دارد.
اعداد کوانتومی
مکانیک موجی که نظریه شرودینگر اساس آن میباشد با استفاده از چهار عدد کوانتومی وضعیت الکترون را توصیف میکند. این اعداد عبارتند از :
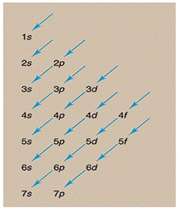
عدد کوانتومی اصلی
این عدد نشاندهنده ترازهای انرژی است که الکترونها در آن ترازها به دور هسته گردش میکنند و عدد صحیحی میباشد. این عدد میتواند کلیه مقادیر اعداد صحیح مثبت به جز صفر را قبول کند.
عدد کوانتومی اندازه حرکت زاویهای مداری
آرنولد زمر فیلد در سال 1916 پیشنهاد کرد که هر مدار بور (n) با شرط n>1 از لایههایی فرعی با اختلاف انرژی کم تشکیل شدهاست. به هر لایه فرعی یک عدد کوانتومی (L) نسبت داده میشود. این عدد نشان دهنده شکل هندسی توزیع تابع احتمال پیدا کردن الکترون در فضای اطراف هسته میباشد و کلیه مقادیر L=0,1,2, … , n-1 را اختیار کند.
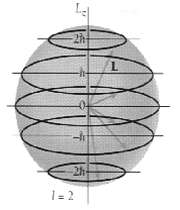
عدد کوانتومی مغناطیسی مداری
تعداد اوربیتالهای یک تراز فرعی را میتوان از این عدد استنتاج کرد که در اثر میدان مغناطیسی هر تراز (L ) به این ترازها شکافته میشود.
به عنوان مثال میدان مغناطیسی بر اوربیتال کروی S که با عدد L=0 مشخص میشود، تاثیری ندارد چون S تقارن کروی دارد و در تمام جهتها بطور یکسان تحت تاثیر خطوط نیرو قرار میگیرد. این عدد که با m نشان داده می شود، مقادیر ممکن این عدد عبارتند از : m=+L,…,0,…,-L
عدد کوانتومی مغناطیسی اسپینی
این عدد مشخص کننده حرکت تقدیمی الکترون است و با نشان داده میشود، و میتواند مقادیر-1/2,+1/2 را اختیار کند.
ابر الکترونی و مکان الکترون
در مورد یک الکترون در حالت n=1 اتم هیدروژن، ابر باردار بالاترین چگالی را در نزدیکی هسته دارد و به تدریج که فاصله از هسته افزایش مییابد، رقیقتر میشود. احتمال یافتن الکترون در حجم کوچکی از فضا، در نزدیکی هسته، بیشترین مقدار را دارد و با افزایش فاصله از هسته به سمت صفر میل میکند.
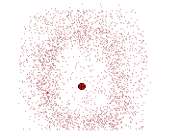
لایههای کروی بسیار نازکی را که یکی پس از دیگری به طور متحدالمرکز به دور هسته قرار دارند، تصور کنید. احتمال یافتن الکترون در واحد حجم فضای نزدیک به هسته بیش ترین مقدار خود را دارد. ولی در عوض یک لایه نزدیک به هسته، در مقایسه با لایههای دورتر، تعداد کم تری واحد حجم را در بر میگیرد. احتمال شعاعی هر دو این عوامل را با هم به حساب میآورد.
انواع اوربیتال
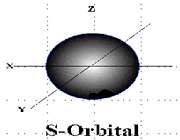
اوربیتال S
اوربیتالهای S دارای تقارن کروی میباشد، تراز n=1 حداکثر دارای دو الکترون است. بنابراین تراز فرعی 1S و 2S و 3S و... هم تقارن کروی دارند، با این تفاوت که اندازه آن ها بزرگتر از اوربیتال 1S میباشد.
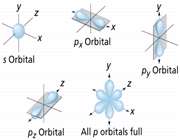
اوربیتال p
اوربیتال p از سه اوربیتال فرعی تشکیل شده است. هر اوربیتال p به شکل دو کره تغییر شکل یافته است که میتوان آن ها را در امتداد یکی از محورهای سه گانه مختصات ( z,y,x) تصور کرد از این رو اوربیتالهای p را با مشخص میکنند که در سه جهت مختلف قرار گرفتهاند.
اوربیتالهای p از لحاظ انرژی برابرند و در غیاب میدان مغناطیسی نمیتوان تفاوتی بین الکترونهایی که این اوربیتالها را اشغال کردهاند، قایل شد. ولی در بررسیهای طیفی که تحت تأثیر یک میدان مغناطیسی قرار میگیرند. هر اوربیتال به سه خط شکافته میشوند.
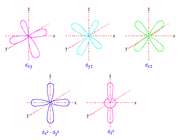
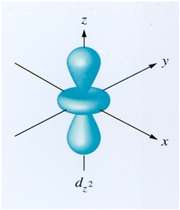
اوربیتال d
اوربیتالهای d از 5 اوربیتال فرعی تشکیل شدهاند که جهت گیریهای متفاوتی در فضا دارند ولی از لحاظ انرژی باهم همارز هستند.
درجه انحطاط
تعداد الکترون هایی که مقدار انرژی برابر داشته باشند، درجه انحطاط یا چندگانگی نامیده میشوند. حداکثر تعداد الکترون های هر تراز از فرمول 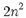 بدست می آید.
بدست می آید.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
حقایقی درباره الماس
با مطالعه حقایق مربوط به الماس، به اطلاعاتی چون الماس های خون گرفته تا فن آوری در زمینه الماس مصنوعی ( ترکیبی ) پی ببرید. از ویژگی های الماس اطلاع حاصل کنید و به کاربردهای آن، ساختار و اتم ها و جواهرات تا زمینه های مختلف اطلاعات و حقایق دیگری به دست بیاورید.

 الماس یکی دیگر از اشکال کربن است.
الماس یکی دیگر از اشکال کربن است. الماس از کلمه یونانی به معنای شکست ناپذیر گرفته شده است.
الماس از کلمه یونانی به معنای شکست ناپذیر گرفته شده است.
 اتم های کربن موجود در الماس در یک ساختار محکم و پیوندی چهارگانه قرار گرفته اند.
اتم های کربن موجود در الماس در یک ساختار محکم و پیوندی چهارگانه قرار گرفته اند.
 الماس سخت ترین ماده طبیعی شناخته شده است که در برش های صنعتی و ابزار صیقل دادن مورد استفاده قرار می گیرد.
الماس سخت ترین ماده طبیعی شناخته شده است که در برش های صنعتی و ابزار صیقل دادن مورد استفاده قرار می گیرد.
 در درجه مقیاس سختی مواد معدنی ( Mohs ) ، الماس شماره 10 را به خود اختصاص داده است که در این مقیاس 1 به نرم ترین ماده ( که طلا است ) و 10 به سخت ترین ماده که الماس است تعلق دارد.
در درجه مقیاس سختی مواد معدنی ( Mohs ) ، الماس شماره 10 را به خود اختصاص داده است که در این مقیاس 1 به نرم ترین ماده ( که طلا است ) و 10 به سخت ترین ماده که الماس است تعلق دارد.
 درمقایسه با دیگر مواد موجود در طبیعت الماس یکی از بهترین هادی های حرارتی است.
درمقایسه با دیگر مواد موجود در طبیعت الماس یکی از بهترین هادی های حرارتی است.
 تحت شرایط عادی، فشار و دمای موجود در سطح زمین، الماس به طور دما پویا بی ثبات است و به آسانی تبدیل به گرافیت می شود. بله درست متوجه شده اید الماس ها تبدیل به گرافیت می شوند. اما مراحل این تبدیل به قدری آهسته صورت می گیرد که ما متوجه آن نمی شویم.
تحت شرایط عادی، فشار و دمای موجود در سطح زمین، الماس به طور دما پویا بی ثبات است و به آسانی تبدیل به گرافیت می شود. بله درست متوجه شده اید الماس ها تبدیل به گرافیت می شوند. اما مراحل این تبدیل به قدری آهسته صورت می گیرد که ما متوجه آن نمی شویم.
 اکثر ذخایر طبیعی موجود الماس در افریقا قرار دارد.
اکثر ذخایر طبیعی موجود الماس در افریقا قرار دارد.
 هرساله حدود 26000 کیلوگرم معادل (57000 پوند ) در سراسر دنیا الماس استخراج می شود که ارزش آن ها برای کمپانی های پر قدرتی که تولید الماس را تحت کنترل دارند میلیون ها دلار است.
هرساله حدود 26000 کیلوگرم معادل (57000 پوند ) در سراسر دنیا الماس استخراج می شود که ارزش آن ها برای کمپانی های پر قدرتی که تولید الماس را تحت کنترل دارند میلیون ها دلار است.
بعد از سنگ Jemstone ، الماس یکی از پرطرفدارترین سنگ هاست که متناوباً در جواهراتی مثل انگشتر و گردنبند استفاده می شود علاوه بر نایاب بودن الماس، این سنگ به آسانی در جواهرات جایگزین می شود، به راحتی قابل براق شدن است و تنها توسط الماسی دیگر قابل خراشیدن است.
 الماس ها بادقت قابل ملاحظه ای بریده شده تا هر قطعه خاص از الماس جلای خیره کننده و قابل توجهی داشته باشد.
الماس ها بادقت قابل ملاحظه ای بریده شده تا هر قطعه خاص از الماس جلای خیره کننده و قابل توجهی داشته باشد.
 هر الماس به نسبت برش آن ها، رنگ، عیار و شفافیت قیمت گذاری می شود.
هر الماس به نسبت برش آن ها، رنگ، عیار و شفافیت قیمت گذاری می شود.
 طی سال ها الماس های زیادی که بسیار گران قیمت نیز بوده اند معروف شده اند که چهارتای آن ها به ترتیب زیر است.
طی سال ها الماس های زیادی که بسیار گران قیمت نیز بوده اند معروف شده اند که چهارتای آن ها به ترتیب زیر است.
 الماس کوه نور که در هند پیدا شد و زمانی فکر می کردند که بزرگترین الماس دنیا است . الان بخشی از جواهرات تاج ملکه انگلیس است که در تاور لندن قرار دارد.
الماس کوه نور که در هند پیدا شد و زمانی فکر می کردند که بزرگترین الماس دنیا است . الان بخشی از جواهرات تاج ملکه انگلیس است که در تاور لندن قرار دارد.
 الماس Hope (آرزو ) که قیرات آن 52/45 است و به دلیل وجود برون (Boroun) در ساختار کریستالی آن به رنگ آبی است.
الماس Hope (آرزو ) که قیرات آن 52/45 است و به دلیل وجود برون (Boroun) در ساختار کریستالی آن به رنگ آبی است.
 درمعدن کیمبرلی در جنوب افریقا ، الماس زرد رنگ تیفانی به وزن حیرت انگیز 42/287 پیدا شد که بعدها به خریدار جواهری به نام چارلز تیفنی در نیویورک فروخته شد و بعدها آن را به شکل بالشتکی به عیار 54/128 (معادل 708/25 گرم ) و 90 تراش برای نشان دادن زیبایی آن برش دادند.
درمعدن کیمبرلی در جنوب افریقا ، الماس زرد رنگ تیفانی به وزن حیرت انگیز 42/287 پیدا شد که بعدها به خریدار جواهری به نام چارلز تیفنی در نیویورک فروخته شد و بعدها آن را به شکل بالشتکی به عیار 54/128 (معادل 708/25 گرم ) و 90 تراش برای نشان دادن زیبایی آن برش دادند.
 این الماس توسط یک برده در یکی از معدن های هند پیدا شد 64/140 قیرات داشت. (1/28 گرم ) این الماس که Regret نامیده شد، درگیر با یک داستان حماسی که در آن یک تاجر دریایی انگلیسی و یک شاهزاده فرانسوی دخیل بودند شد.
این الماس توسط یک برده در یکی از معدن های هند پیدا شد 64/140 قیرات داشت. (1/28 گرم ) این الماس که Regret نامیده شد، درگیر با یک داستان حماسی که در آن یک تاجر دریایی انگلیسی و یک شاهزاده فرانسوی دخیل بودند شد.
الآن در موزه لوور فرانسه از سال 1887 به معرض نمایش گذاشته شده است.

 الماس در فرم طبیعی آن بیلیون ها سال تحت فشار و گرمای زیاد طول می کشد تا شکل بگیرد. آن ها اغلب با یک فوران آتش نشانی به روی سطح زمین آورده می شوند.
الماس در فرم طبیعی آن بیلیون ها سال تحت فشار و گرمای زیاد طول می کشد تا شکل بگیرد. آن ها اغلب با یک فوران آتش نشانی به روی سطح زمین آورده می شوند.
 در سال 1940 تحقیقاتی درباره تکنولوژی الماس ترکیبی صورت گرفت ودرسال 1950اولین الماس ترکیبی تولید شد.
در سال 1940 تحقیقاتی درباره تکنولوژی الماس ترکیبی صورت گرفت ودرسال 1950اولین الماس ترکیبی تولید شد.
 شیوه های مختلفی برای ایجاد الماس ترکیبی وجود دارد که شامل ترکیب فشار زیاد و دمای زیاد ، تبخیر شیمیایی و انفجار ترکیبی ( منفجر کردن واقعی کربن برای به وجود آمدن دانه های بسیار ریز الماس ).
شیوه های مختلفی برای ایجاد الماس ترکیبی وجود دارد که شامل ترکیب فشار زیاد و دمای زیاد ، تبخیر شیمیایی و انفجار ترکیبی ( منفجر کردن واقعی کربن برای به وجود آمدن دانه های بسیار ریز الماس ).
 این ماده ترکیبی که به عنوان مربع زیرکونیا شناخته شده است یک شکل کریستالی از دی اکسید زیرکونیوم است (ZrO2) . به دلیل ویژگی هایش که علاوه بر سختی آن، بدون عیب و بدون رنگ بودن آن، همچنین ارزان و بادوام نیز هست الماس نام گرفته است.
این ماده ترکیبی که به عنوان مربع زیرکونیا شناخته شده است یک شکل کریستالی از دی اکسید زیرکونیوم است (ZrO2) . به دلیل ویژگی هایش که علاوه بر سختی آن، بدون عیب و بدون رنگ بودن آن، همچنین ارزان و بادوام نیز هست الماس نام گرفته است.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
حقایقی در باره نیتروژن
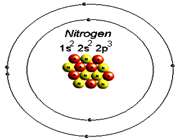
حقایق جالب توجه مربوط به نیتروژن را مطالعه کنید و درباره گازی که هوای قابل تنفس برای شما را فراهم می سازد بیش تر بدانید.
نیتروژن عنصری خارق العاده است که دارای ویژگی های منحصر به فرد است و در مواد منفجره، داروهای بیهوشی، باروری، و هم چنین مسابقات ماشین سواری مورد استفاده قرار می گیرد.
با مطالعه حقایق جالب توجه در باره اتم نیتروژن، نیتروژن مایع ، اکسید نیتروژن اسید نیتریک و نیتروگلیسرین و چیزهای دیگر آگاه شوید.
 نیتروژن عنصری شیمیایی با علامت اختصاری N است که عدد اتمی آن 7 می باشد.
نیتروژن عنصری شیمیایی با علامت اختصاری N است که عدد اتمی آن 7 می باشد. تحت شرایط معمولی نیتروژن گازی بدون رنگ، بو و مزه است .
تحت شرایط معمولی نیتروژن گازی بدون رنگ، بو و مزه است .

 نزدیک به 78% از هوایی که تنفس می کنیم از نیتروژن تشکیل شده است.
نزدیک به 78% از هوایی که تنفس می کنیم از نیتروژن تشکیل شده است.
 نیتروژن در همه موجودات زنده از جمله بدن انسان و گیاهان وجود دارد.
نیتروژن در همه موجودات زنده از جمله بدن انسان و گیاهان وجود دارد.
نیتروژن برای نگه داشتن طولانی مدت غذا به صورت بسته بندی و یا فله کاربرد دارد. هم چنین برای ساخت قطعات  الکترونیکی، اهداف صنعتی و بسیاری مقاصد مفید دیگر استفاده دارد.
الکترونیکی، اهداف صنعتی و بسیاری مقاصد مفید دیگر استفاده دارد.
 بیش از 98% اتمسفری که تیتان (TITAN ) بزرگ ترین ماه زحل را دربر گرفته است از نیتروژن تشکیل شده است. در منظومه خورشیدی ما تنها این ماه است که دارای اتمسفری متراکم است.
بیش از 98% اتمسفری که تیتان (TITAN ) بزرگ ترین ماه زحل را دربر گرفته است از نیتروژن تشکیل شده است. در منظومه خورشیدی ما تنها این ماه است که دارای اتمسفری متراکم است.

 در دمای پایین نیتروژن به صورت مایع است. نیتروژن مایع در77 کلوین معادل (196- درجه سانتیگراد و 321- درجه فارنهایت ) به راحتی قابل جابه جایی است و کاربردهای زیادی دارد. نگهداری مواد در دمای پایین، در زمینه علم برودت شناسی ) علمی که در آن به عکس العمل مواد در دمای بسیار پایین می پردازد )، هم چنین به عنوان عامل سرد کننده در کامپیوتر ( مایعی که از آن استفاده می شود تا از بالا رفتن دما در کامپیوتر جلوگیری کند)، ازبین برنده زگیل نیز بوده و بسیاری چیزهای دیگر.
در دمای پایین نیتروژن به صورت مایع است. نیتروژن مایع در77 کلوین معادل (196- درجه سانتیگراد و 321- درجه فارنهایت ) به راحتی قابل جابه جایی است و کاربردهای زیادی دارد. نگهداری مواد در دمای پایین، در زمینه علم برودت شناسی ) علمی که در آن به عکس العمل مواد در دمای بسیار پایین می پردازد )، هم چنین به عنوان عامل سرد کننده در کامپیوتر ( مایعی که از آن استفاده می شود تا از بالا رفتن دما در کامپیوتر جلوگیری کند)، ازبین برنده زگیل نیز بوده و بسیاری چیزهای دیگر.
 در بیماری کم فشاری ( که به آن بندز نیز گفته می شود ) نیتروژن به صورت حباب هایی درون رگ های انتقال خون و دیگر قسمت های مهم بدن ایجاد می شود که در آن شخص به هنگام غواصی به طور ناگهانی دچار بی فشاری می شود مشابه با چیزی که فضانوردان و یا کسانی که در هواپیماهای کم فشار کار می کنند با آن رو به رو می شوند.
در بیماری کم فشاری ( که به آن بندز نیز گفته می شود ) نیتروژن به صورت حباب هایی درون رگ های انتقال خون و دیگر قسمت های مهم بدن ایجاد می شود که در آن شخص به هنگام غواصی به طور ناگهانی دچار بی فشاری می شود مشابه با چیزی که فضانوردان و یا کسانی که در هواپیماهای کم فشار کار می کنند با آن رو به رو می شوند.
 اکسید نیتروس (که به آن گاز خنده آور نیز گفته می شود با فرمول شیمیایی N2O ) در بیمارستان ها وکلینیک های دندانپزشکی به عنوان بیهوش کننده مورد استفاده قرار می گیرد . (در جراحی های مختلف به عنوان از بین برنده و کاهش دهنده درد و هوشیاری عمومی کاربرد دارد.)
اکسید نیتروس (که به آن گاز خنده آور نیز گفته می شود با فرمول شیمیایی N2O ) در بیمارستان ها وکلینیک های دندانپزشکی به عنوان بیهوش کننده مورد استفاده قرار می گیرد . (در جراحی های مختلف به عنوان از بین برنده و کاهش دهنده درد و هوشیاری عمومی کاربرد دارد.)
 اکسید نیتروس هم چنین در مسابقات موتورسواری برای افزایش قدرت موتور و سرعت وسیله نقلیه استفاده می شود که در این صورت به آن نیتروس یا NOS گفته میشود .
اکسید نیتروس هم چنین در مسابقات موتورسواری برای افزایش قدرت موتور و سرعت وسیله نقلیه استفاده می شود که در این صورت به آن نیتروس یا NOS گفته میشود .
 اکسید نیتروس یکی از گازهای گلخانه ای قابل توجه واز آلاینده های هوا است . تاثیر آن از نظر وزنی 300 برابر بیشتر از دی اکسید کربن است.
اکسید نیتروس یکی از گازهای گلخانه ای قابل توجه واز آلاینده های هوا است . تاثیر آن از نظر وزنی 300 برابر بیشتر از دی اکسید کربن است.
 نیتروگلیسرین مایعی است که در ایجاد انفجار مانند دینامیت مورد استفاده قرار می گیرد واغلب در صنایع ساخت وساز ونظامی کاربرد دارد.
نیتروگلیسرین مایعی است که در ایجاد انفجار مانند دینامیت مورد استفاده قرار می گیرد واغلب در صنایع ساخت وساز ونظامی کاربرد دارد.
 اسید نیتریک (HNO3) اسیدی قوی است که غالبا در عمل لقاح استفاده می شود.
اسید نیتریک (HNO3) اسیدی قوی است که غالبا در عمل لقاح استفاده می شود.
 آمونیا (HN3 ) یکی دیگر از ترکیبات نیتروژن است که بیش تر در عمل بارورسازی مصرف می شود.
آمونیا (HN3 ) یکی دیگر از ترکیبات نیتروژن است که بیش تر در عمل بارورسازی مصرف می شود.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
حقایقی درباره کربن
کربن نقشی اساسی در دنیای ما ایفا می کند از دی اکسید کربن موجود در هوا گرفته تا گرافیت (کربن ) موجود در مداد شما، همه جا می توانید آثار آن را بیابید. در این مقاله شما می توانید درباره کاربردهای بیشتر کربن، اتم کربن، ویژگی های آن ، هیدروکربن ها، ساختار کربن، بافت کربن ، منوکسید کربن ، ردپای کربن در شما و حقایق جالب توجه دیگر اطلاع کسب کنید.
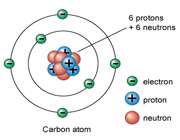
 علامت شیمیایی عنصر کربن C است و عدد اتمی آن 6 می باشد.
علامت شیمیایی عنصر کربن C است و عدد اتمی آن 6 می باشد. کربن از کلمه لاتین کربو به معنای ذغال گرفته شده است.
کربن از کلمه لاتین کربو به معنای ذغال گرفته شده است. کربن تعداد زیادی ترکیب را به وجود می آورد که از ترکیبات دیگر عناصر خیلی بیشتر است. به دلیل توانایی کربن در برقراری پیوند با دیگر عناصر غیر فلزی، اغلب از آن به عنوان ماده سازنده حیات نام می برند.
کربن تعداد زیادی ترکیب را به وجود می آورد که از ترکیبات دیگر عناصر خیلی بیشتر است. به دلیل توانایی کربن در برقراری پیوند با دیگر عناصر غیر فلزی، اغلب از آن به عنوان ماده سازنده حیات نام می برند.
 در حالی که کربن ترکیبات متفاوتی را به وجود می آورد ولی عنصری بدون واکنش است.
در حالی که کربن ترکیبات متفاوتی را به وجود می آورد ولی عنصری بدون واکنش است.
 کربن دارای شکل های متفاوتی است سه نوع آن دارای ساختمانی نامشخص است. (ذغال ، دوده و غیره )، الماس و گرافیت.
کربن دارای شکل های متفاوتی است سه نوع آن دارای ساختمانی نامشخص است. (ذغال ، دوده و غیره )، الماس و گرافیت.
 گرافیت و الماس ویژگی های بسیار متفاوتی دارند. الماس بسیار شفاف و دارای جنسی سخت است. در حالی که گرافیت بسیار نرم و سیاه است ( به اندازه ای نرم است که با آن روی کاغذ می نویسند. )
گرافیت و الماس ویژگی های بسیار متفاوتی دارند. الماس بسیار شفاف و دارای جنسی سخت است. در حالی که گرافیت بسیار نرم و سیاه است ( به اندازه ای نرم است که با آن روی کاغذ می نویسند. )

 از گرافیت به عنوان یک عایق حرارتی استفاده می شود ( گرما را به میزان کم تری منتقل می کند. ) گرافیت هم چنین یک رسانای خوب و الکتریسیته است.
از گرافیت به عنوان یک عایق حرارتی استفاده می شود ( گرما را به میزان کم تری منتقل می کند. ) گرافیت هم چنین یک رسانای خوب و الکتریسیته است.
اتم های کربن در گرافیت به شکل شش ضلعی تخت ولایه به لایه بر روی صفحه قرار گرفته است.
 از نظر فراوانی کربن چهارمین عنصر موجود در جهان است. (بعد از هیدروژن –هلیوم و اکسیژن ). در پوسته زمین پانزدهمین عنصر فراوان موجود است و در بدن انسان دومین عنصر فراوان است. (البته بعد از اکسیژن )
از نظر فراوانی کربن چهارمین عنصر موجود در جهان است. (بعد از هیدروژن –هلیوم و اکسیژن ). در پوسته زمین پانزدهمین عنصر فراوان موجود است و در بدن انسان دومین عنصر فراوان است. (البته بعد از اکسیژن )
 کربن دارای بالاترین درجه ذوب در بین دیگر عناصر است. حدود 3500 درجه سانتیگراد (3773 کلوین و 6332 درجه فارنهایت )
کربن دارای بالاترین درجه ذوب در بین دیگر عناصر است. حدود 3500 درجه سانتیگراد (3773 کلوین و 6332 درجه فارنهایت )
 هیدروکربن ها ترکیبات آلی هستند که از مولکول هایی با خصیصه های هیدروژن و کربن تشکیل شده اند.
هیدروکربن ها ترکیبات آلی هستند که از مولکول هایی با خصیصه های هیدروژن و کربن تشکیل شده اند.
 ساده ترین ترکیب هیدروکربن متان با فرمول شیمیایی ( CH4) است.
ساده ترین ترکیب هیدروکربن متان با فرمول شیمیایی ( CH4) است.
 کربن در تمدن های اولیه انسانی به صورت ذغال چوب و دوده کشف شد.
کربن در تمدن های اولیه انسانی به صورت ذغال چوب و دوده کشف شد.
 «ردپای کربن » جمله ای است که معنای آن در ارتباط با گازهای گلخانه ای منتشر شده توسط یک کشور، موسسه و یاشخص خاصی است.
«ردپای کربن » جمله ای است که معنای آن در ارتباط با گازهای گلخانه ای منتشر شده توسط یک کشور، موسسه و یاشخص خاصی است.
 چرخه کربن فرآیندی است که در آن کربن در همه جای زمین علی الخصوص در سیستم های حیاتی آن رد و بدل می شود.
چرخه کربن فرآیندی است که در آن کربن در همه جای زمین علی الخصوص در سیستم های حیاتی آن رد و بدل می شود.
این امری بسیار مهم و حیاتی روی زمین است که به کربن این امکان را می دهد که پیوسته در حال بازیافت و یا استفاده مجدد باشد.
 |
 دراتمسفر زمین، کربن به صورت دی اکسید کربن (CO2 ) یافت می شود. اگرچه حجم کمی از اتمسفر را اشغال می کند، ولی نقشی اساسی در این باره دارد. از جمله این که توسط گیاهان در زمان فتوسنتز مورد استفاده قرار می گیرد.
دراتمسفر زمین، کربن به صورت دی اکسید کربن (CO2 ) یافت می شود. اگرچه حجم کمی از اتمسفر را اشغال می کند، ولی نقشی اساسی در این باره دارد. از جمله این که توسط گیاهان در زمان فتوسنتز مورد استفاده قرار می گیرد.
 منوکسید کربن (CO ) برای انسان و حیوان بسیار سمی است و در شرایطی که اکسیژن به اندازه کافی برای شکل گیری دی اکسید کربن نیست منوکسید شکل می گیرد. در بسیاری از کشورهای سراسر دنیا مسمومیت با منوکسید کربن یکی از متداول ترین و کشنده ترین مسمومیت هاست.
منوکسید کربن (CO ) برای انسان و حیوان بسیار سمی است و در شرایطی که اکسیژن به اندازه کافی برای شکل گیری دی اکسید کربن نیست منوکسید شکل می گیرد. در بسیاری از کشورهای سراسر دنیا مسمومیت با منوکسید کربن یکی از متداول ترین و کشنده ترین مسمومیت هاست.
 بافت کربن ماده ای بسیار سخت است که از بافت های نازک که عمدتاٌ از اتم های کربن که به صورت کریستال های میکروسکوپی به هم پیوند شده اند و در مواردی که استقامت بالا و وزن کم مورد نیاز است مورد استفاده قرار می گیرد.
بافت کربن ماده ای بسیار سخت است که از بافت های نازک که عمدتاٌ از اتم های کربن که به صورت کریستال های میکروسکوپی به هم پیوند شده اند و در مواردی که استقامت بالا و وزن کم مورد نیاز است مورد استفاده قرار می گیرد.
 سوخت های فسیلی مانند گاز متان ویا نفت خام ( بنزین ) نقش مهمی در اقتصاد مدرن ایفا می کند.
سوخت های فسیلی مانند گاز متان ویا نفت خام ( بنزین ) نقش مهمی در اقتصاد مدرن ایفا می کند.
 پلاستیک از مشتقات پلی مرهای کربن به وجود می آید. کربن به عنوان یک آلیاژ با آهن ترکیب می شود مثل استیل کربن.
پلاستیک از مشتقات پلی مرهای کربن به وجود می آید. کربن به عنوان یک آلیاژ با آهن ترکیب می شود مثل استیل کربن.
 گرافیت و خاک رس برای ساخت مغز مداد استفاده می شود.
گرافیت و خاک رس برای ساخت مغز مداد استفاده می شود.
 ذغال چوب اکثراٌ برای کباب کردن غذا در منقل استفاده می شود.
ذغال چوب اکثراٌ برای کباب کردن غذا در منقل استفاده می شود.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
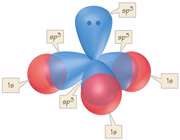
انواع اوربیتال هیبریدی
اوربیتال هیبریدی SP

درگیر شدن تمام اوربیتال های پوسته والانس اتم مرکزی یک مولکول، در تشکیل اوربیتال های هیبریدی ضرورت ندارد. تنها آن تعداد از اوربیتال های مزبور برای تشکیل اوربیتال های هیبریدی مورد استفاده قرار میگیرند که تعداد پیوند لازم و نیز شکل هندسی مولکول را تأمین کنند. برای مثال توابع موجی سه اوربیتال هیبرید را میتوان از ترکیب ریاضی توابع موجی یک اوربیتال S و دو اوربیتال P به دست آورد. یکی از سه اوربیتال P، در این عمل شرکت نمیکند.
اوربیتال هیبریدی SP3
هیبریداسیونSP3 یک نوع مهم و متداول میباشد. این اوربیتالها از هیبرید شدن یک اوربیتال S و 3 اوربیتال P تشکیل میشوند.

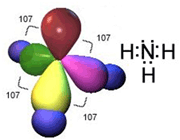
اوربیتال هیبریدی SP3 با یک جفت الکترون غیر پیوندی: در مولکولهایی مانند NH3 میتوان تصور کرد که اتم نیتروژن از اوربیتالهای هیبریدی SP3 استفاده کرده است، که یکی از آن ها توسط یک جفت الکترون غیر مشترک اشغال شده است. اتمهای مولکول یک هرم مثلثی تشکیل میدهند. ولی آرایش 4 اوربیتال N تقریباً به صورت یک 4 وجهی است و زاویه پیوند تقریبا برابر با 107 درجه میباشد.
اوربیتال هیبریدی SP3 با دو جفت الکترون غیر پیوندی: اتم اکسیژن هم در مولکول H2O از اوربیتالهای SP3 استفاده میکند که در آن دو اوربیتال هیبریدی توسط دو جفت الکترون غیر مشترک اشغال شدهاند. زوایای اتم و 104/5 0 میباشد که این زاویه به 1090 نزدیک تر است تا به 900 ، که در صورت به کار رفتن اوربیتال خالصP، انتظار میرفت.
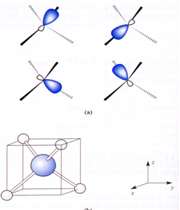
اوربیتال هیبریدی دارای اوربیتال d
اوربیتالهای d2SP3 : این اوربیتالها از هیبرید شدن 2 اوربیتال d و یک اوربیتال s و 3 اوربیتال p به وجود میآیند.
هر 6 اوربیتال با یکدیگر همارز بوده و به سوی گوشههای یک هشت وجهی منتظم جهت گیری دارند. یک نوع از این ها با یک جفت الکترون غیر پیوندی (این اوربیتال دارای شکل هرم، با قاعده مربع) بوده و نوع دیگرش با دو جفت الکترون غیر پیوندی (این اوربیتال دارای شکل مربع مسطح) میباشد.

اوربیتال اتمی dx2 - y2: در تشکیل این اوربیتال هیبریدی دخالتی ندارد. پنج اوربیتال حاصل با یکدیگر همارز نیستند. این اوربیتالها در گوشههای یک دو هرمی مثلثی جای میگیرند. زاویه بین پیوندهایی که در قاعده قرار گرفتهاند 1200 و پیوندهای خارج از قاعده 900 و زاویهای که دو راس هرم را به هم وصل میکند 1800 میباشد.

نکات مهم در هیبریداسیون اوربیتالها
• محاسبات نشان میدهد که استفاده از اوربیتالهای هیبریدی به تشکیل پیوندهای قوی تر منجر میشود.
• انرژی لازم برای ایجاد حالت برانگیخته و هم چنین انرژی لازم برای هیبرید شدن، بیش تر از انرژی آزاد شده به هنگام تشکیل دو پیوند نسبتا قوی کوالانسی است.
• اوربیتالهایی که در آن ها دو نوع معینی از هیبریداسیون به کار رفته است، باید از لحاظ انرژی نسبتا به هم نزدیک باشند.
• اوربیتالهایی که معمولاً در تشکیل پیوند به کار میروند اوربیتالهای d , p , s لایه خارجی و در برخی موارد اوربیتال d لایه ماقبل لایه خارجی هستند. به استثنای این اوربیتالهای d داخلی، الکترونهای اوربیتالهای داخلی معمولاً آن قدر به هسته وابسته هستند که نمیتوانند در تشکیل پیوند شرکت کنند.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
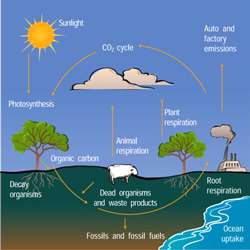
چرخه شناسایی آب
در اتمسفر زمین سیستم گردش آب به طور پیوسته وجود دارد. در درون این چرخه، جریان آب از سمت زمین به سوی اتمسفر و مجددا با برگشت به سوی زمین صورت می گیرد.
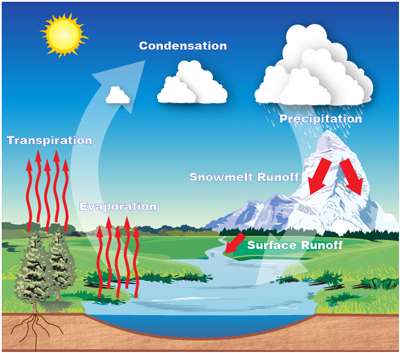 |
اگرچه مراحل زیادی در شکل گیری این چرخه وجود دارند ولی مهم ترین آن ها به شرح ذیل می باشند.
- تبخیر
- فراتراوش
- میعان
- بارش
- جاری شدن
تبخیر
به تغییر فرم ماده، از حالت مایع به حالت گاز تبخیر می گوییم. در علم هواشناسی ماده مورد نظر آب می باشد. برای این که تبخیری صورت بگیرد نیازمند مقداری انرژی هستیم.
این انرژی را از منابع متعددی مثل خورشید، اتمسفر، زمین و یا موجودات روی زمین مانند انسان می توان گرفت. همه ما تجربه هایی پیرامون موضوع تبخیر داریم . هنگامی که دمای بدن ما در اثر گرمای هوا و یا ورزش کردن بالا می رود بدن عرق کرده و آب روی پوست ظاهر می شود.
این اتفاق به این دلیل می افتد که بدن از گرمای درون خودش برای تبخیر مایع استفاده می کند و به این ترتیب گرما از بین رفته و بدن سرد می شود. هم چنین هنگامی که شما از زیر دوش یا استخر بیرون می آیید همان تاثیر را می بینید. احساس خنکی شما به دلیل رفع گرمای بدن برای ایجاد بخار آب روی پوست (عرق) است.
فراتراوش (بخار کردن )
به تبخیر آب از طریق منافد گیاهان عمل (فراتراوش – تنفس ) گفته می شود. منافذ به دریچه های ریزی گفته می شود که در زیر برگ وجود دارد و به بافت آوندی گیاه متصل شده اند. در اکثر گیاهان، عمل فراتراوش طی مراحلی که اغلب توسط رطوبت اتمسفر و نم موجود در خاک کنترل می شود، صورت می گیرد. فقط یک درصد از آبی که از طریق ریشه وارد گیاه می شود، جهت مراحل رشد مورد استفاده گیاه قرار می گیرد. مابقی آن که 99 درصد می باشد وارد اتمسفر می شود.
میعان
در عمل میعان، بخار آبی که در اتمسفر وجود دارد تبدیل به مایع می شود. در اتمسفر میعان به شکل ابر و یا شبنم مشاهده می شود. وقتی که آب بر دیواره قوطی ویا بطری نوشابه ای که بدون درپوش است می نشیند در اصطلاح می گوییم میعان رخ داده است.
میعان در یک دمای خاص اتفاق نمی افتد بلکه معمولا در اختلاف بین دو دما شکل می گیرد. مانند تفاوتی که بین دمای هوا و نقطه شبنم وجود دارد. در یک بیان ساده نقطه شبنم به دمایی که شبنم در آن شکل می گیرد گفته می شود. در واقع دما نقش مهمی در این مورد ایفا می کند به این صورت که اگر هوا به سطح مشخصی از سرما برسد اشباع می شود. هر نوع افزایش در آن دما باعث تبدیل بخار آب به مایع می شود.
اغلب هنگامی که دمای هوا و دمای نقطه تشکیل شبنم برابر شود مه تشکیل می شود. میعان نقطه مقابل تبخیر است. از آنجایی که بخار آب نسبت به آب، در حالت مایع، از سطح انرژی بالاتری برخوردار است، هنگامی که میعان صورت می گیرد، انرژی اضافی به شکل انرژی گرمایی آزاد می شود. این آزاد سازی گرما در شکل گیری گردباد نقش دارد.
بارش
هنگامی که قطرات کوچک در میعان به هم می پیوندند، و به قطرات بزرگ تری تبدیل می شوند، قطرات باران ایجاد می شود که با افزایش تراکم قطرات بارش، به سمت زمین فرو می ریزد.
بارش به صورت های مختلف مثل باران، تگرک، برف و یا باران دیده می شود.
بارش یکی از ساده ترین راه ها برای دریافت آب تازه در زمین است. به طور میانگین خشکی ها و دریاهای کره زمین سالانه حدود 5/38 اینچ (980 میلی لیتر ) آب از طریق بارندگی دریافت می کنند.
جاری شدن آب
وقتی بارش ها از حد ظرفیت زمین بیش تر شوند و زمین اشباع گردد،( یعنی دیگر آب را به خود جذب نکند )، عمل جاری شدن آب اتفاق می افتد. رودخانه ها ودریاچه ها در اثر این جریان آب به وجود می آیند. در حرکت آب به سوی رودخانه ها و دریاچه ها مقداری عمل تبخیر هم صورت می گیرد ولی بیشتر آب به اقیانوس ها برمی گردد.
اگر آب به گونه ای باشد که فقط وارد دریاچه شود و دریاچه خروجی نداشته باشد تا آب از آن خارج شود، تنها راه بازگشت آب به اتمسفر تبخیر آن است. با عمل تبخیر، تنها آب خالص بخار می شود و بنابراین هر گونه آلودگی و نمک برجای خواهد ماند ودر نهایت دریاچه نمکی خواهیم داشت.
در تبخیر آب به سوی اتمسفر ، جریان آب دوباره برقرار می شود. قسمتی از آب به درون خاک و زمین نفوذ می کند تا دوباره توسط گیاهان جذب شده و عمل پس دادن بخار (فرا تراوش ) صورت بگیرد.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
تولید مثل

همه ی جاندارانی كه پیرامون ما هستند یا تك سلولی و یا پر سلولی هستند هر یك از این جانداران توانایی دارند كه هم نوع خود را به وجود آورند. به عبارت دیگر تولید مثل كنند.
اهمیت تولید مثل:

همه ی موجودات زنده برای بقای خود فعالیت هایی مانند: تنفس كردن، رشد كردن، .... انجام می دهند. اما یكی از مهم ترین كارهای موجودات زنده فعالیت در جهت بقای نسل خود است.
اگر جانداری نتواند فعالیت غیر تولید مثل انجام دهد از بین می رود اما اگر این گونه از جانداران نتوانند فعالیت تولید مثل انجام دهد نسل جاندار منقرض خواهد شد. بقای نسل در جاندار به عوامل ارثی محیطی جاندار مربوط می شود.
توانایی مقاومت یك جاندار در برابر بیماری ها، شكار شدن، عوامل محیطی، آب و هوا، تغییرات دما، بلایای طبیعی مانند زلزله، سیل، آتشفشان از جمله عوامل محیطی و ارثی هستند.

در تولید مثل غیر جنسی، جاندار به مرحله ای از رشد خود كه می رسد می تواند تكثیر شود و افراد جدیدی را به وجود آورد. بسیاری از جانداران ساده كه ساختمان بدنی ساده ای دارند و برخی گیاهان به این روش زیاد می شوند مانند: باكتری ها، تك سلولی ها، برخی گیاهان و جانداران.
در روش تولید مثل غیر جنسی همه ی جانداران تكثیر یافته یك گونه و كاملا مانند هم بوده و خصوصیات ساختمانی و حیاتی یكسانی دارند. در این جانداران اگر شرایط محیطی تغییر كند و این شرایط برای جاندار مضر باشد همه ی نسل آن ها از بین می رود.

دونیم شدن:
در این روش یك جاندار مانند: آسیب تقسیم می شود و به جاندار كه از نظر اندازه تقریبا ساده است تبدیل می شود.
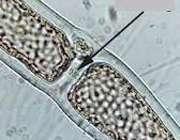
جوانه زدن:
بعضی از جانداران مانند هیدر به این روش زیاد می شوند در این روش برآمدگی كوچكی در بدن جاندار ایجاد می شود و كم كم به جانداری مستقل تبدیل شده و ممكن است از بدن جاندار اولیه جدا شود یا هم چنان متصل باقی بماند مانند: هیدر آب شیرین و مخمرنان.
قطعه قطعه شدن:
در این روش، بدن جاندار به چندین قطعه تقسیم می شود. سپس بعضی، یا همه ی آن ها به جاندار بالغ تبدیل می شوند. مثلا جلبك اسپیروژیر با این روش زیاد می شود. این گیاهان نیز با روش تولید مثل غیرجنسی زیاد می شوند.
تولید مثل رویشی در گیاهان به دو طریق طبیعی و مصنوعی صورت می گیرد.

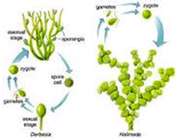
ساقه زیر زمینی:
بعضی از گیاهان با ساقه زیر زمینی زیاد می شوند،ساقه های زیر زمینی كلروفیل ندارند و دارای برگ های قهوه ای فلس مانند دارند.

ریزم:
ریزم تقریبا به صورت افقی در خاك رشد می كند در انتهای این ساقه ها جوانه انتهای وجود دارد، مانند مهد سلیمان.
غده:
غده به منزله ی انتهای ساقه است كه دارای اندوخته غذایی است مانند سیب زمینی.
پیاز:
در پیاز تعدادی برگ بدون سبزینه وجود دارد كه اطراف جوانه قرار دارد. (مانند پیاز خوراكی) سنبل.

بنه:
بنه نسبت به پیاز ساقه بزرگ تری دارد اما فاقد فلس های متعدد است، مانند: زعفران و گلایل.
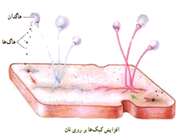
هاگزایی:
در این روش تولید مثل هاگ به وجود می آید هاگ یك سلول ویژه است كه توسط جاندار اولیه تولید می شود. و به تنهایی و به طور مستقیم جاندار به وجود می آورد. مثلا در كپك نان هاگ ها در اندام هایی به نام هاگدان تولید می شود. پس از رسیدن هاگ در هاگدان، هاگدان پاره می شود و هاگ ها همراه باد و آب به نقاط مختلف می روند.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:
تولید مثل ( 2)
در مقاله ی گذشته مطالبی در رابطه با تولید مثل دانستیم. در این ادامه خواهیم دانست...
تولید مثل جنسی:
در این روش تولید مثل، باید دو نوع سلول جنسی نر و ماده وجود داشته باشد. این سلول ها با هم تركیب شده و اولین سلول جاندار جدید كه سلول تخم نام دارد به وجود می آید.
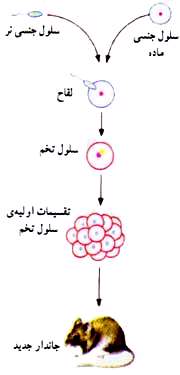
بنابر این در روش تولید مثل جنسی، گامت نر (سلول جنسی نر) و گامت ماده (سلول جنسی ماده) در اندام های تولید مثل نر و ماده تولید می شود و از تركیب آن ها سلول تخم به وجود آید. به تركیب شدن سلول نر و ماده لقاح می گویند.
تولید مثل جنسی در گیاهان گل دار:
بیشتر گیاهان با كاشتن دانه زیاد می شوند و دانه ها توسط گل ها تشكیل می شوند.
گل اندام تولید مثلی در گیاهان گل دار است. در گیاهان پیدایش گل موجب آغاز دوره ی جدید (تولید مثل جنسی گیاه) است. نقش گل، تشكیل گامت ها و فراهم كردن شرایط تركیب آن ها با یكدیگر است.
بعضی از گل ها ممكن است یك یا چند بخش دانه داشته باشند كه به آن ها گل ناقص می گویند.
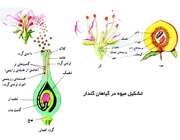 هنگامی كه دانه گرده در درون بساك پرچم كامل می شود كیسه بساك پاره شده و دانه ها پراكنده می شوند و توسط عوامل مختلف مانند باد، حشرات و ... پراكنده می شوند.
هنگامی كه دانه گرده در درون بساك پرچم كامل می شود كیسه بساك پاره شده و دانه ها پراكنده می شوند و توسط عوامل مختلف مانند باد، حشرات و ... پراكنده می شوند.

چنان چه دانه ی گرده ی یك گل، روی كلاله مادگی همان گل بیفتد، گردافشانی را مستقیم، و چنان چه دانه گرده ای روی كلاله مادگی گل دیگر از همان نوع قرار گیرد گرده افشانی را غیر مستقیم می گویند.
در درون دانه ی گرده دو نوع هسته رویشی و زایشی وجود دارد. از تقسیم شدن هسته زایشی سلول جنسی نر (گامت نر) به وجود می آید.
گامت نر با گامت ماده ی موجود در تخمدان تركیب می شود و سلول تخم به وجود می آید. سلول تخم، درون تخمك قرار دارد تبدیل به دانه و تخمدان تبدیل به میوه می شود.
بنابر این میوه، تخمدان رشد كرده و رسیده ی گل است كه ممكن است قسمت های دیگر گل را نیز به همراه داشته باشد. میوه ی موجب حفاظت از دانه و موجب پراكندگی و زمانبندی لازم برای رویش دانه می شود.
تولید مثل جنسی در جانوران:
در جانداران نیز مانند گیاهان سلول جنسی نر (اسپرم) در اندام تولید مثلی نر (بیضه) و سلول جنسی ماده تخمك در اندام تولید مثلی ماده به وجود می آید. در همه ی مهره داران و بعضی از بی مهره ها اندام تولید مثلی نر و ماده در دو جاندار جدا از هم وجود دارد، اما مانند اسفنج ها، مرجان ها، بعضی كرم ها، نرم تنان.
در بعضی از جانداران ساده تر:
روش تولید مثل جنسی در جانداران متفاوت است اما دو ویژگی مشترك در این روش ها وجود دارد.
(كامت نر و ماده باید با هم برخورد كنند و تركیب شوند و سلول تخم به وجود آید.)


تولید مثل در انسان:
تولید مثل در انسان نیز مانند سایر پستانداران با تشكیل سلول جنینی نر (اسپرم) بیضه و سلول جنسی ماده یا تخمك در تخمدان و تركیب هسته های آن ها با یكدیگر و ایجاد سلول تخم صورت می گیرد.
غدد جنسی در مردان بیضه و در زنان تخمدان نام دارد. وظایف غدد جنسی تولید گامت و هورمون های جنسی است.
بیضه:
بیضه ها شامل یك جفت غده هستند كه در زیر شكم و درون كیسه بیضه قرار دارند. این غدد شامل لوله های نازك و پرپیچ و خمی هستند كه به لوله های اسپرم ساز موسومند. این لوله ها عمل اسپرم سازی از دوران بلوغ شروع می كنند و تا پایان عمر ادامه می دهند.
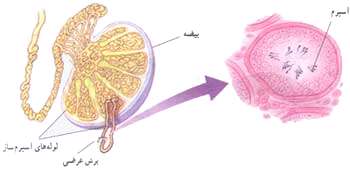
تخمدان ها شامل دو عدد غده ی بیضی شكل است كه در دو طرف داخل شكم، در پایین و جلوی روده ها قرار دارند تخمدان ها، تخمك سازی را ازدوران بلوغ شروع كرده و تا حدود 30 الی 40 سالگی ادامه می دهند.
معمولا هر ماه یك تخمك نارس فعال می شود و به یك تخمك كامل تبدیل می شود این سلول به و سیله ی لوله های فالوب به دورن رحم انتقال می یابد و چنان چه با سلول نر یا اسپرم تركیب شود به سلول تخم تبدیل می شود تخم با تقسیمات خود جنین را به وجود می آورد كه از طریق جفت با خون مادر ارتباط غذایی پیدا می كنند.
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:






 آمار
وب سایت:
آمار
وب سایت:

